Привет, Вы узнаете о том , что такое соотношение числа и состава исходных веществ и продуктов реакции, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое
соотношение числа и состава исходных веществ и продуктов реакции, изменение степени окисления атомов, выделение или поглощение теплоты, направление протекания реакции, участие катализатора, наличие границы раздела фаз , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Реактивы: цинк, железо, медь и уголь; кислоты серная и хлороводородная; гидроксиды натрия и кальция; соли калия — хлорид, сульфат и карбонат; соли меди(II) — сульфат и хлорид; фенолфталеин.
Проведите химические реакции согласно заданиям 1–4, составьте уравнения реакций и охарактеризуйте каждую из них по признакам:
- 1)
соотношение числа и состава исходных веществ и продуктов реакции ;
- 2)
изменение степени окисления атомов ;
- 3)
выделение или поглощение теплоты ;
- 4)
направление протекания реакции ;
- 5)
участие катализатора ;
- 6)
наличие границы раздела фаз (см. § 18).
В уравнениях окислительно-восстановительных реакций расставьте коэффициенты. Укажите окислители и восстановители.
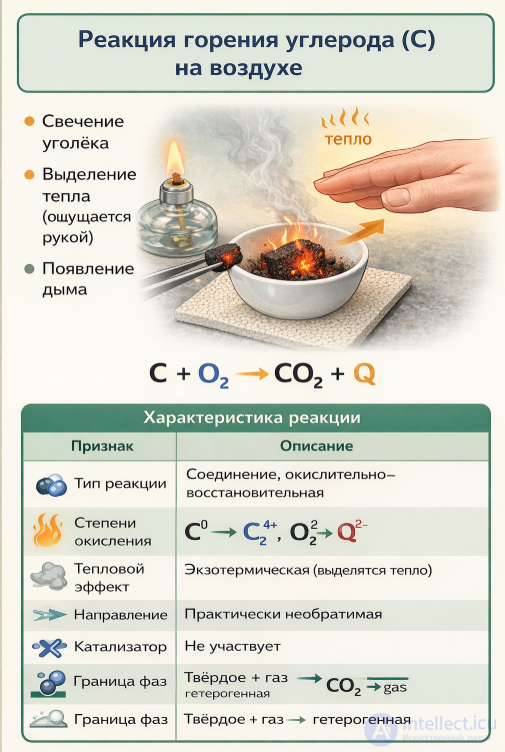
Задание 1. Раскалите в пламени спиртовки уголек, воспользовавшись пинцетом. Положите уголек в фарфоровую чашку. Через некоторое время поднесите к нему ладонь, ощутите выделение теплоты. Отметьте признаки реакции.
Задание 2. Раствор щелочи с 1–2 каплями индикатора нейтрализуйте кислотой.
Задание 3. Проведите реакцию соли меди(II) с имеющимся металлом.
Задание 4. Проведите любые две реакции между имеющимися у вас сложными веществами.
Задание 1. Раскалите в пламени спиртовки уголек, воспользовавшись пинцетом. Положите уголек в фарфоровую чашку. Через некоторое время поднесите к нему ладонь, ощутите выделение теплоты. Отметьте признаки реакции.
Задание 1. Нагревание уголека (углерода) на воздухе
Наблюдения
- уголек раскаляется и тлеет
- выделяется тепло (ощущается рукой)
- может наблюдаться слабое свечение
- образуется газ (углекислый газ, без запаха)
Уравнение реакции
(Q — выделение теплоты)

Характеристика реакции по признакам
- Соотношение числа и состава веществ
- из двух веществ образуется одно
- это реакция соединения
- Изменение степеней окисления
- C⁰ → C⁴⁺ (в CO₂) — углерод окисляется
- O₂⁰ → O²⁻ — кислород восстанавливается
реакция окислительно-восстановительная
Окислитель: O₂
Восстановитель: C
- Тепловой эффект
- выделяется тепло
реакция экзотермическая
- Направление протекания
- реакция практически необратимая (идет до конца при доступе кислорода)
- Катализатор
- Граница раздела фаз
- углерод — твердое вещество
- кислород — газ
реакция гетерогенная (есть граница фаз)
Итог
Это реакция соединения, окислительно-восстановительная, экзотермическая, необратимaя, гетерогенная, без катализатора.
Задание 2. Раствор щелочи с 1–2 каплями индикатора нейтрализуйте кислотой.
К раствору щелочи (например, NaOH) добавляют 1–2 капли индикатора (фенолфталеин), затем приливают кислоту (например, HCl) до изменения окраски.
Уравнение реакции
Молекулярное:
Полное ионное:
Сокращенное ионное:
Характеристика реакции
1) Соотношение веществ
- Два вещества → два продукта
реакция обмена (двойного замещения)
2) Степени окисления
- Na: +1 → +1
- Cl: −1 → −1
- H: +1 → +1
- O: −2 → −2
не изменяются → не ОВР
3) Тепловой эффект
Реакция сопровождается выделением тепла
(экзотермическая)
4) Направление реакции
Реакция идет до конца, так как образуется слабый электролит — вода
5) Катализатор
не требуется
6) Граница раздела фаз
Все вещества в растворе
гомогенная реакция
Наблюдения (индикатор)
- Фенолфталеин:
- в щелочи → малиновый
- после добавления кислоты → обесцвечивается
признак нейтрализации
Вывод
Это типичная реакция нейтрализации:
- обменная
- не ОВР
- экзотермическая
- необратимая
- протекает в растворе
Задание 3. Об этом говорит сайт https://intellect.icu . Проведите реакцию соли меди(II) с имеющимся металлом.
Для соли меди(II) можно взять любой более активный металл из набора: цинк или железо (медь не реагирует, уголь — только при нагревании).
Ниже — пример с цинком (самый наглядный опыт)
Реакция соли меди(II) с цинком
(например, раствор сульфата меди(II))
Уравнение реакции:
Электронный баланс (ОВР)
- Zn⁰ − 2e⁻ → Zn²⁺ (окисление)
- Cu²⁺ + 2e⁻ → Cu⁰ (восстановление)
Окислитель: Cu²⁺ (ион меди)
Восстановитель: Zn (цинк)
Характеристика реакции по признакам
1) Соотношение числа и состава веществ
- Реакция замещения
- Один металл вытесняет другой из соли
2) Изменение степеней окисления
- Zn: 0 → +2 (окисляется)
- Cu: +2 → 0 (восстанавливается)
Это окислительно-восстановительная реакция
3) Тепловой эффект
- Реакция экзотермическая (выделяется теплота)
4) Направление протекания
- Реакция необратимая, идет до конца
- Причина: более активный металл вытесняет менее активный
5) Участие катализатора
6) Наличие границы раздела фаз
- Реакция гетерогенная
- Граница:
Наблюдения в опыте
- Голубой раствор постепенно обесцвечивается
- На цинке появляется красный налет меди
- Цинк постепенно растворяется
Если взять железо
Характеристика аналогичная, только:
- Fe — восстановитель
- раствор становится зеленым (FeSO₄)
Задание 4. Проведите любые две реакции между имеющимися у вас сложными веществами.
Нужно выбрать две реакции между сложными веществами (кислоты, щелочи, соли) и охарактеризовать их. Вот готовый пример оформления.
Реакция 1 Между кислотой и щелочью (реакция нейтрализации)
Уравнение:
Характеристика реакции
- Соотношение числа и состава веществ
Реакция обмена (двойного замещения). Образуется соль и вода.
- Изменение степеней окисления
Степени окисления не меняются → не ОВР.
- Тепловой эффект
Реакция экзотермическая (выделяется тепло)
- Направление реакции
Идет до конца, т.к. образуется слабый электролит — вода.
- Катализатор
Катализатор не требуется.
- Граница раздела фаз
Все вещества в растворе → реакция гомогенная.
Реакция 2 Между солью и щелочью (образование осадка)
Уравнение:
(выпадает голубой осадок гидроксида меди(II))
Характеристика реакции
- Соотношение числа и состава веществ
Реакция обмена (двойного замещения), образуется осадок.
- Изменение степеней окисления
Cu²⁺ → Cu²⁺ (не меняется)
ОВР отсутствует.
- Тепловой эффект
Слабый тепловой эффект, практически без заметного выделения тепла.
- Направление реакции
Идет до конца, так как образуется нерастворимое вещество — осадок.
- Катализатор
Катализатор не требуется.
- Граница раздела фаз
Есть граница фаз: раствор + твердый осадок → реакция гетерогенная.
Вывод:
- Обе реакции — реакции обмена
- Не являются окислительно-восстановительными
- Первая идет из-за образования воды
- Вторая идет из-за образования осадка
Исследование, описанное в статье про соотношение числа и состава исходных веществ и продуктов реакции, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое соотношение числа и состава исходных веществ и продуктов реакции, изменение степени окисления атомов, выделение или поглощение теплоты, направление протекания реакции, участие катализатора, наличие границы раздела фаз
и для чего все это нужно, а если не понял, или есть замечания,
то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории
Неорганическая химия
Из статьи мы узнали кратко, но содержательно про соотношение числа и состава исходных веществ и продуктов реакции


Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия