Лекция
Привет, Вы узнаете о том , что такое состояние электрона, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое состояние электрона , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Развитие квантовой механики в 20-х годах ХХ века привело к коренному пересмотру фундаментальных понятий теории строения атома. Исследование свойств электрона показало, что ему присущи свойства как частицы, так и волны. Электрон как частица характеризуется массой и электрическим зарядом, как волна — длиной волны, которая зависит от скорости движения электрона. Эту двойственность свойств электрона назвали корпускулярно-волновым дуализмом.

Рис. 15. Пленка, состоящая из наночастиц Au и SnO2:
а — изображение, б — дифракционная картина.
Фотографии получены методами, основанными
на использовании волновых свойств электронов
В настоящее время волновые свойства электрона используются в электронной и атомно-силовой микроскопии, позволяющей рассматривать различные объекты (размером порядка 10–9 м) с увеличением в сотни тысяч раз (рис. 15). Без этих методов было бы невозможным появление нанотехнологий.
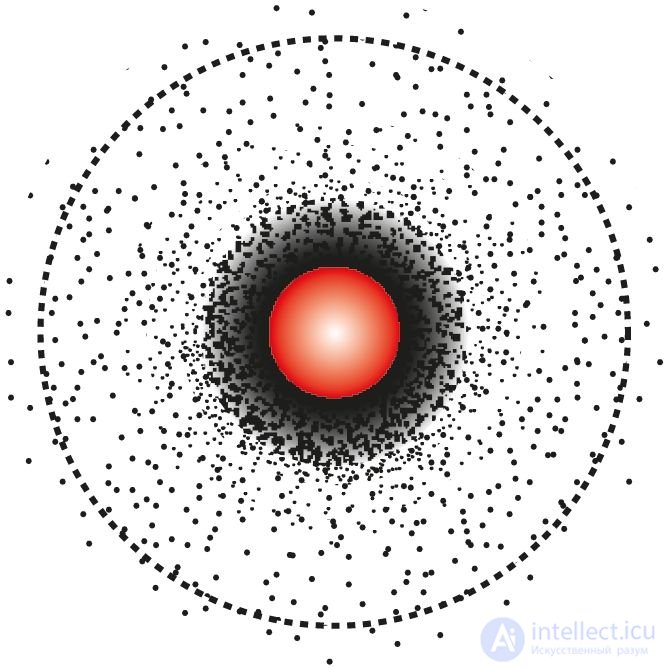
Рис. 16.
Электронное
облако атома
водорода
С точки зрения квантовой механики для электрона нельзя одновременно точно определить его координату и скорость, а следовательно, невозможно проследить траекторию движения электрона в атоме, поэтому говорят о вероятности нахождения электрона в определенной области пространства около ядра. Ее ограничивают условной поверхностью, охватывающей примерно 90 % объема, в котором наиболее велика вероятность нахождения данного электрона (рис. 16). Такую область околоядерного пространства называют атомной электронной орбиталью, или просто атомной орбиталью.
Каждому электрону в атоме соответствует своя атомная орбиталь, которая характеризуется определенными значениями энергии, формой и размером электронного облака.
За условный размер атомной s-орбитали принимают диаметр облака, в котором вероятность нахождения данного электрона составляет примерно 90 % (см. пунктирную линию на рис. 16).
По форме электронного облака различают s-, p-, d- и f-орбитали. s-Орбитали имеют форму сферы, р — форму гантели, d и f — более сложную форму (рис. 17).

Рис. 17. Форма электронных облаков s-, p-орбиталей (верхняя строка)
и d-орбиталей (нижняя строка)
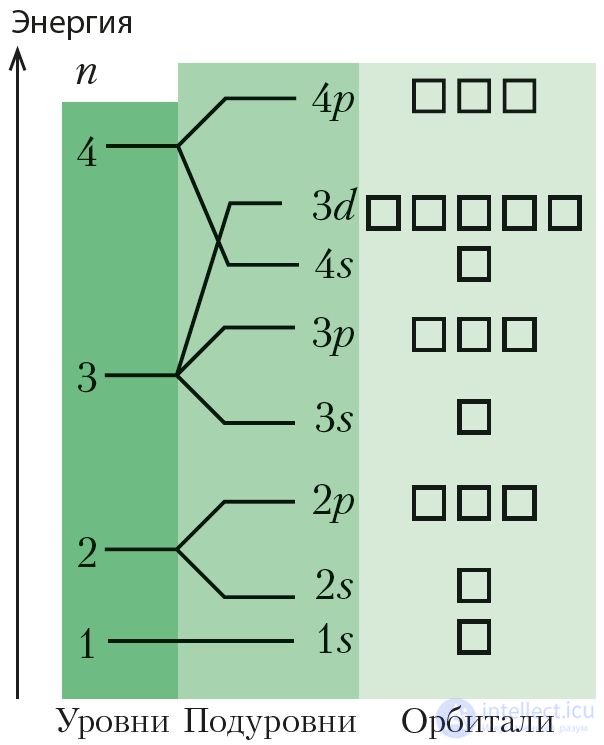
Рис. 18. Схема распределения
атомных орбиталей по энергии
(энергетическая диаграмма)
Согласно основному принципу квантовой механики, электрон в атоме может принимать только определенные значения энергии, а другие значения запрещены. В этом случае говорят, что энергия электрона квантована, то есть имеет дискретный набор значений. Для наглядного представления состояний электронов в атоме используют энергетическую диаграмму (рис. 18). Проанализируем этот рисунок. Из рисунка следует, что электроны в атоме распределены по энергетическим уровням и подуровням.
Энергетические уровни (или электронные слои, с которыми вы ознакомились, изучая химию в 9-м классе) обозначают числом n. Это число имеет только целочисленные значения: 1, 2, 3, … Каждому значению n соответствует определенное значение энергии электрона. Энергия может изменяться только скачкообразно. Самый низкий энергетический уровень (n = 1) соответствует минимально возможной энергии электрона. Находящиеся на этом уровне электроны наиболее сильно связаны с ядром. Чем больше n, слабее его связь с ядром, больше размер электронного облака, тем больше энергия электрона. При n = ∞ электрон теряет связь с ядром и считается свободным.
Вам уже известно, что число электронов на энергетических уровнях различно. Так, на первом энергетическом уровне может быть не более 2, на втором — не более 8, на третьем — не более 18 электронов.
Число электронов, которое может вместить определенный уровень, можно вычислить по формуле:
N(e–) = 2n2.
Электроны, находящиеся на одном энергетическом уровне, образуют электронную оболочку, или слой. Высшую по энергии электронную оболочку называют внешней. На ней расположены электроны, которые слабее всего связаны с ядром и поэтому способны участвовать в образовании химических связей. Их называют валентными.
В многоэлектронных атомах энергетические уровни расщепляются на энергетические подуровни (табл. 5). На первом уровне (n = 1) есть только один подуровень — 1s, на втором (n = 2) — два подуровня (2s и 2p), на третьем — их три (3s, 3p и 3d).
Таблица 5. Распределение электронов в атоме по уровням, подуровням, орбиталям
| Энергетический уровень, n | Подуровень | Число атомных орбиталей | Максимальное число электронов на подуровне | Максимальное число электронов на энергетическом уровне (N(e–) = 2n2) |
| 1 | 1s | 1 | 2 | 2 |
| 2 |
2s 2p |
1 3 |
2 6 |
8 |
| 3 |
3s 3p 3d |
1 3 5 |
2 6 10 |
18 |
*f-Электронные облака

Существует 7 f-атомных орбиталей, на которых может разместиться 14 электронов. Об этом говорит сайт https://intellect.icu . Им соответствует 7 электронных облаков, форма которых представлена на рисунке 17.1.
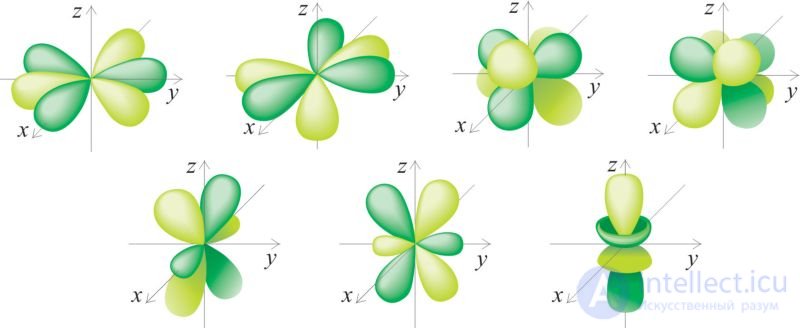
Рис. 17.1. Форма электронных облаков f-орбиталей
Атомные орбитали, порядок их заполнения электронами
На энергетической диаграмме атомные орбитали изображены в виде клеток (ячеек): (рис. 18). На каждом энергетическом подуровне может находиться только определенное число одинаковых по энергии атомных орбиталей: на любом s-подуровне — одна
, на p — три
, на d — пять
.
Как вам уже известно, на каждой атомной орбитали может разместиться не более двух электронов: , причем электроны должны отличаться своими спинами. Спин условно характеризует вращение электрона вокруг собственной оси по часовой стрелке или против нее. Эти различия у электронов на схеме изображают стрелками, направленными в противоположные стороны. Если на орбитали находится один электрон
, его называют неспаренным, а атомную орбиталь — наполовину заполненной. Если на орбитали два электрона
, то электроны называют спаренными, а орбиталь — заполненной. Атомную орбиталь без электронов называют вакантной, или свободной
.
Вместимость энергетических уровней показана в таблице 5.
Вам известны три способа изображения распределения электронов в атоме:
1) в виде электронных схем (показывают распределение электронов только по энергетическим уровням), например для углерода 6С 2е–, 4е–;
2) в виде формулы электронной конфигурации (показывают распределение электронов по орбиталям), например 6С 1s22s22p2, где цифры перед буквами s и p указывают номер энергетического уровня, буквы s и p — форму электронного облака, а верхний индекс над буквами — число электронов, размещенных на подуровне;
3) с помощью электронно-графических схем (показывают распределение электронов по орбиталям с учетом спина электрона), например:
6C 
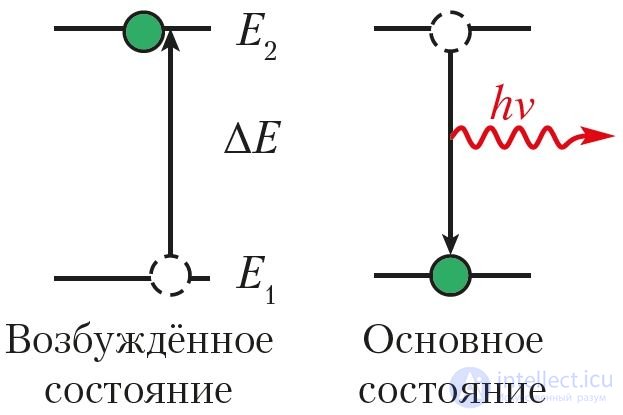
Рис. 19. Схема перехода электрона
из основного в возбужденное
состояние
Электронно-графическая схема — это та же энергетическая диаграмма, но с изображением заполнения электронами атомных орбиталей.
Состояние атома с наименьшей возможной для него энергией электронов называют основным, или невозбужденным, состоянием. Все другие энергетические состояния этого атома, которым соответствует бо́льшая энергия электронов, чем в основном состоянии, называются возбужденными.
Для того чтобы перевести атом в возбужденное состояние, ему надо сообщить энергию — энергию возбуждения (ΔE) (рис. 19). Она передается при воздействии на атом электромагнитного излучения (например, солнечного света), при нагревании или воздействии на атом быстрых электронов. В основном состоянии атом может находиться неограниченно долго, а в возбужденном — около 10–15 с, после чего возбужденные электроны возвращаются в основное состояние. Переход атома из возбужденного состояния в основное сопровождается электромагнитным излучением.

Электрону присущи свойства как частицы, так и волны.
Атомная орбиталь — это характеристика состояния электрона в атоме, которая включает определенное значение энергии, форму и размер электронного облака.
Электронное строение атома характеризуют с помощью электронной схемы, формулы электронной конфигурации и электронно-графической схемы.
Вопросы, задания, задачи
1. Назовите характеристики электрона:
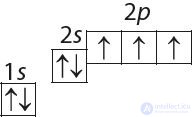
2. Назовите способы изображения распределения электронов в атоме азота:
3. Как изменится энергия электрона, если его перевести из состояния с n = 2 в состояние с n = 3? Что произойдет с энергией электрона, если он вернется в прежнее состояние?
4. Используя рис. 18, расположите следующие атомные орбитали в порядке увеличения их энергии: 3p, 2p, 3d, 1s.
5. В каком состоянии энергия электрона выше: 2s или 2p; 3p или 2p?
6. Чем отличаются атомные орбитали 1s и 3s?
7. Сколько всего электронов может находиться на третьем энергетическом уровне, на 1s-подуровне, на 2р-подуровне, на 3d-подуровне?
8. При возбуждении электрон перешел с 2s- на 2р-орбиталь. Что при этом изменилось: энергия электрона, форма электронного облака, заряд атома, энергия атома?
9. Рассчитайте число электронов в порции фосфора массой 1,24 г.
10. Порция нитрата двухвалентного металла количеством 0,2 моль содержит 16,4 моль электронов. Определите элемент.

*Самоконтроль
1. Корпускулярно-волновой дуализм рассматривает электрон только как:
2. Укажите изображения р-орбитали:
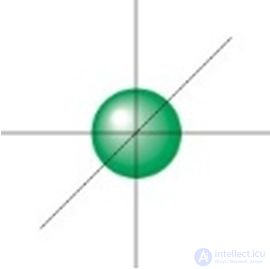

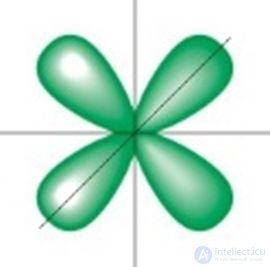
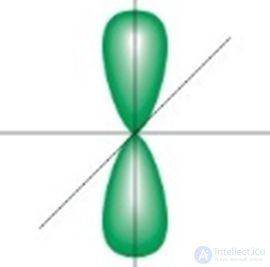
3. Электронно-графической схемой атома углерода в основном состоянии является:
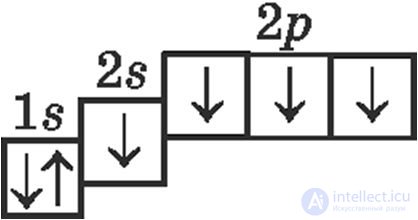
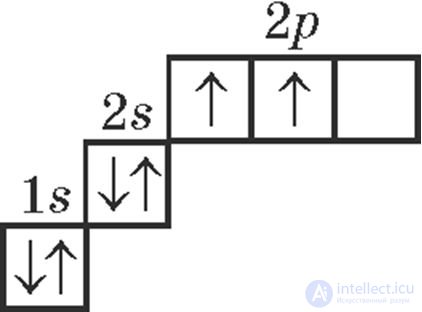

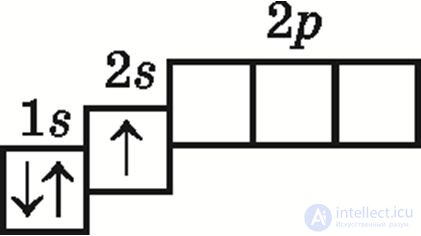
4. Правильными являются утверждения:
5. В порядке увеличения энергии атомные орбитали указаны в рядах:
Исследование, описанное в статье про состояние электрона, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое состояние электрона и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия