Лекция
Неметаллы — химические элементы, как правило, не обладающие свойствами металлов. Занимают правый верхний угол Периодической системы элементов Менделеева и обычно отделены линией (лесенкой). Количество неметаллов составляет 22-23 элемента, в зависимости от классификации.
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов и проявлению более высокой окислительной активности, чем у металлов.
Считаются двадцать три элемента неметаллами, Четырнадцать элементов практически всегда признаются таковыми: водород, кислород, азот и сера; коррозионно-активные галогены: фтор, хлор, бром и иод; и благородные газы: гелий, неон, аргон, криптон, ксенон и радон; а так же углерод, фосфор и селен
Опишите признаки реакций. Укажите анионы, входящие в состав полученных осадков.
Разберем обе реакции по шагам.
Уравнение реакции:
Признак реакции:
— образуется белый нерастворимый осадок.
Что это за осадок:
— сульфат бария
Анион в составе осадка:
— (сульфат-ион)
Уравнение реакции:
Признак реакции:
— образуется белый творожистый осадок (может темнеть на свету).
Что это за осадок:
— хлорид серебра
Анион в составе осадка:
— (хлорид-ион)
В первой реакции осадок содержит анион
Во второй реакции осадок содержит анион

Вот как выполнить качественные реакции для определения состава веществ
Нужно доказать наличие:
катиона NH₄⁺ (аммоний)
аниона Cl⁻ (хлорид)
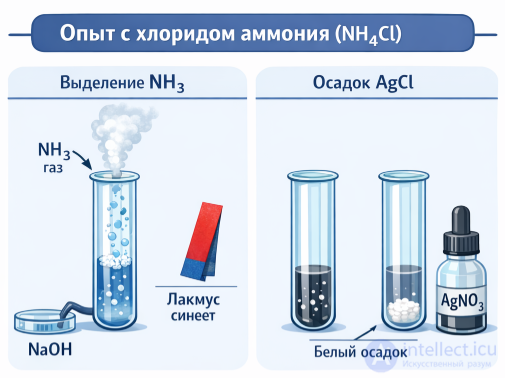
Реакция с щелочью (NaOH):
NH₄Cl + NaOH → NH₃↑ + NaCl + H₂O
Признаки:
выделяется газ аммиак (NH₃) с резким запахом
влажная красная лакмусовая бумага синеет
Реакция с нитратом серебра (AgNO₃):
NH₄Cl + AgNO₃ → AgCl↓ + NH₄NO₃
Признаки:
образуется белый осадок AgCl (хлорид серебра)
Нужно доказать наличие:
катиона H⁺
аниона SO₄²⁻ (сульфат)
Реакция с металлом (например, Zn):
Zn + H₂SO₄ → ZnSO₄ + H₂↑
Признаки:
выделяется газ водород (H₂)
слышен «пшик», пузырьки газа
Реакция с хлоридом бария (BaCl₂):
H₂SO₄ + BaCl₂ → BaSO₄↓ + 2HCl
Признаки:
образуется белый нерастворимый осадок BaSO₄ (сульфат бария)

NH₄Cl → NH₃ (газ) + AgCl (осадок)
H₂SO₄ → H₂ (газ) + BaSO₄ (осадок)
Разберем задание — как различить растворы с помощью качественных реакций.
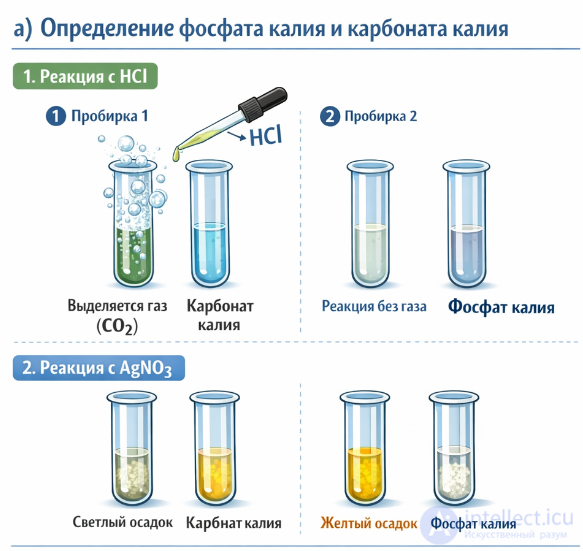
1. Реакция с кислотой (например, HCl)
Карбонат калия:
Признак: выделяется газ (пузырьки CO₂)
Фосфат калия:
Признак: газа нет
Вывод:
Есть пузырьки → карбонат
Нет пузырьков → фосфат
2. Дополнительная реакция (с AgNO₃)
Фосфат:
Желтый осадок
Карбонат:
Светло-желтый осадок (менее устойчивый)
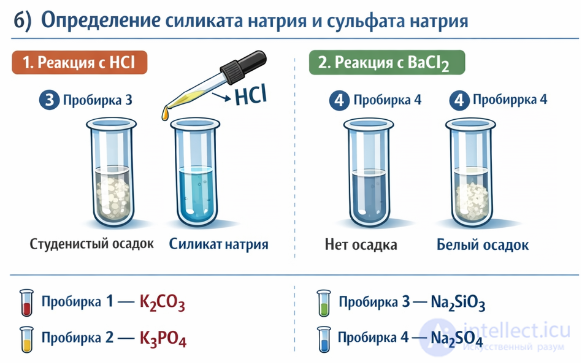
1. Реакция с кислотой (HCl)
Силикат натрия:
Признак: образуется студенистый (гелеобразный) осадок кремниевой кислоты
Сульфат натрия:
Признак: никаких изменений
Вывод:
Есть гель → силикат
Нет изменений → сульфат
2. Подтверждение (реакция с BaCl₂)
Сульфат:
Белый нерастворимый осадок
Силикат:
Белый осадок (но растворяется в кислоте)
Итог
| Вещество | Реакция | Признак |
|---|---|---|
| K₂CO₃ | +HCl | газ CO₂ |
| K₃PO₄ | +HCl | нет газа |
| Na₂SiO₃ | +HCl | гель |
| Na₂SO₄ | +BaCl₂ | белый осадок |
Рассчитайте и сравните питательную ценность выданных удобрений.
При составлении отчета о работе уравнения реакций, протекающих в растворах, представьте в молекулярной и ионной формах.
Решение
Вот как можно опытным путем определить вещества в пробирках
Добавь щелочь (например, NaOH) и слегка нагрей:
Признак:
появляется резкий запах аммиака → это сульфат аммония
Реакция:
Газ можно проверить влажной красной лакмусовой бумагой — она синеет.
Если запаха аммиака нет, значит это кальциевая селитра (Ca(NO₃)₂).
Дополнительно можно подтвердить:
Добавь раствор карбоната натрия (Na₂CO₃):
Признак:
белый осадок карбоната кальция
(поташ = K₂CO₃)
Проверка на карбонат (CO₃²⁻)
Добавь кислоту (например, HCl):
Признак:
выделяется газ (CO₂), идет шипение → это поташ
CO₂ можно подтвердить:
пропустить через известковую воду → она помутнеет
Определение хлорида калия
Если газа нет, значит это хлорид калия (KCl).
Дополнительно можно проверить:
Добавь раствор нитрата серебра (AgNO₃):
Признак:
белый осадок AgCl
Краткая таблица
| Вещество | Реактив | Признак |
|---|---|---|
| (NH₄)₂SO₄ | NaOH + нагрев | запах NH₃ |
| Ca(NO₃)₂ | Na₂CO₃ | белый осадок |
| K₂CO₃ | HCl | выделение CO₂ |
| KCl | AgNO₃ | белый осадок |

сульфат аммония → по запаху аммиака
кальциевая селитра → по осадку CaCO₃
поташ → по выделению CO₂
хлорид калия → по осадку AgCl
Питательная ценность определяется содержанием основных элементов: N (азот), K (калий), Ca (кальций).
Молярная масса:
Ca = 40
N₂ = 28
O₆ = 96
M = 164 г/моль
Азот:
Содержит ~17% азота + кальций (Ca)
Очень ценное удобрение (рост + укрепление растений)
Молярная масса:
N₂ = 28
H₈ = 8
S = 32
O₄ = 64
M = 132 г/моль
Азот:
Содержит ~21% азота + серу (S)
Более богат азотом
Молярная масса:
K = 39
Cl = 35.5
M ≈ 74.5 г/моль
Калий:
~52% калия
Очень концентрированное калийное удобрение
Молярная масса:
K₂ = 78
C = 12
O₃ = 48
M = 138 г/моль
Калий:
~56% калия
Чуть более богат калием, чем KCl
Сравнение
| Удобрение | Основной элемент | Содержание |
|---|---|---|
| (NH₄)₂SO₄ | N | ~21% |
| Ca(NO₃)₂ | N | ~17% |
| KCl | K | ~52% |
| K₂CO₃ | K | ~56% |
по азоту: сульфат аммония > кальциевая селитра
по калию: поташ > хлорид калия
Выводы к работе
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия