Лекция
Привет, Вы узнаете о том , что такое растворение, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое растворение , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Вы уже знакомы со смесями веществ — растворами и механическими смесями, их классификацией (рис. 50). Напомним, что механические смеси образуются в результате простого перемешивания веществ без образования ими химической связи или других химических изменений. Каждый компонент такой механической (гетерогенной) смеси сохраняет свой состав и свойства.

Рис. 50. Классификация смесей
Также вам уже известны растворы — гомогенные устойчивые системы переменного состава, состоящие из нескольких компонентов. Различают жидкие (водные и неводные), газообразные и твердые растворы. Некоторые их примеры приведены на рисунке 50. Мы будем рассматривать преимущественно водные растворы.
В отличие от механических смесей растворы однородны, то есть отсутствуют границы раздела фаз. Кроме того, растворы устойчивы, так как при неизменных условиях (концентрация растворенного вещества, температура, давление) они бесконечно долго остаются гомогенными системами.
Физико-химический процесс, при котором происходит взаимодействие частиц растворяемого вещества и растворителя с образованием гомогенной устойчивой системы переменного состава, называют растворение м.
Химическая сторона процесса растворения заключается в разрушении связей между частицами растворяемого вещества и их взаимодействии с молекулами растворителя. При растворении протекают физические процессы взаимной диффузии частиц растворяемого вещества и молекул воды.
Растворитель — это компонент раствора, агрегатное состояние которого не изменяется при образовании раствора.
В жидких растворах и смесях газов растворитель — обычно компонент, количество которого в растворе преобладает. Тем не менее в водных растворах, независимо от концентрации растворенного вещества, растворителем считают воду, например раствор серной кислоты с массовой долей 98 %, медицинский спирт с массовой долей этанола 97 %.
В твердых веществах могут быть растворены газы, жидкости или другие твердые вещества. Так, в металлах хорошо растворяется газообразный водород: 900 объемов в одном объеме палладия при 80 °С. В одном объеме платины при 450 °С растворяется около 70 объемов кислорода. Эти твердые растворы обладают повышенной каталитической активностью во многих окислительно-восстановительных процессах.
Образование твердых растворов высокомолекулярных соединений с жидкими пластификаторами имеет важное значение в химии полимеров. Например, в присутствии пластификаторов жесткий поливинилхлорид, из которого делают оконные рамы и виниловый сайдинг, превращается в гораздо более гибкий материал, что позволяет изготавливать из него шланги, оболочку электрических кабелей и т. п.
Образование твердых растворов происходит при легировании металлов и их сплавов — добавлении в состав основного материала небольших количеств особых примесей для улучшения его физических и химических свойств: износостойкости, прочности, пластичности, коррозионной стойкости. Полупроводниковые материалы на основе твердых растворов незаменимы в производстве изделий электронной техники.
Пример газообразного раствора — это воздух, представляющий собой смесь газообразных кислорода, азота, углекислого газа и благородных газов, паров воды, в которой преобладает азот.
Примерами жидких растворов являются нефть — смесь жидких углеводородов, уксус — раствор уксусной кислоты в воде. Вода — самый распространенный растворитель. Главной причиной проявления водой свойств хорошего растворителя, в частности солей и молекулярных соединений с полярными связями, является строение ее полярных молекул, представляющих собой диполи. Растворяющие свойства воды значительно усиливает ее способность образовывать межмолекулярные водородные связи с полярными молекулами.
Итак, жидкие и твердые растворы — это не механическая смесь частиц растворителя и растворенного вещества, а продукт физико-химических процессов, в результате которых исчезает межфазная граница и образуется гомогенная система.
По мере растворения вещества его концентрация в растворе повышается, а сам процесс замедляется. В насыщенном растворе избыток нерастворенного вещества находится в подвижном равновесии с раствором: скорость растворения частиц вещества равна скорости их возвращения из раствора обратно в исходную фазу (газ, жидкость или кристалл).
Между частицами растворенного вещества и растворителя имеет место электростатическое взаимодействие. Оно реализуется при растворении в воде электролитов — солей, щелочей и др., когда полярные молекулы воды связываются силами кулоновского притяжения с катионами и анионами электролита.
Межмолекулярное взаимодействие растворенного вещества и растворителя может происходить посредством образования водородных связей, например, между молекулами воды и спиртов, аминов, аммиака и др.
Взаимодействие молекул растворителя и частиц растворяемого вещества имеет определяющее значение. Так, гелий — это газ, состоящий из самых маленьких атомов, и одновременно наименее растворимый в воде газ. Следовательно, растворимость вещества — это не способность его частиц размещаться между молекулами воды (или иного растворителя), а способность с ними взаимодействовать.
Для разрыва химических связей между частицами растворяемого вещества необходимо затратить энергию. Следовательно, количество теплоты в системе убывает и первая стадия растворения — это эндотермический процесс. При связывании частиц растворяемого вещества и растворителя на второй стадии процесса растворения энергия, наоборот, выделяется. Это экзотермический процесс, количество теплоты возрастает. Суммарный тепловой эффект процесса растворения равен сумме двух величин:
Q(растворения) = –Q(разрыв химических связей) + Q(образование химических связей).
Экспериментальные данные показывают, что при растворении твердых веществ в одних случаях теплота выделяется, а в других — поглощается. Например, при растворении в воде нитрата аммония NH4NO3 наблюдается сильное охлаждение раствора. Причина заключается в том, что количество теплоты, выделяющейся при взаимодействии катионов и анионов
с молекулами воды, меньше количества теплоты, затрачиваемой на разрыв ионных связей в кристаллах нитрата аммония (Q(растворения) = –26,4 кДж/моль). Другой пример — растворение в воде гидроксида калия, которое сопровождается сильным разогреванием раствора. В этом случае энергия, выделяемая при взаимодействии ионов K+ и OH– с молекулами воды, больше, чем энергия, затрачиваемая на разрыв связей между этими ионами в кристаллическом KOH (Q(растворения) = +55,6 кДж/моль).
Растворение газов и жидкостей в воде обычно сопровождается выделением теплоты, так как практически отсутствуют затраты энергии на разрушение связей между молекулами исходного вещества.
Как правило, хорошо растворяются друг в друге подобные по физическим и химическим свойствам вещества, то есть действует эмпирическое правило «подобное растворяется в подобном». Например, вещества, состоящие из полярных молекул, и вещества с ионным типом химической связи хорошо растворяются в полярных растворителях (вода, этанол). Неполярные вещества хорошо растворяются в неполярных растворителях (бензол, толуол).
Нерастворимые газы (например, He, Ne, H2, N2, CO) имеют растворимость менее 2 см3/100 г воды. Об этом говорит сайт https://intellect.icu . Нерастворимыми в воде являются многие твердые вещества: оксиды (например, CuO, ZnO, Fe2O3, Cr2O3, Al2O3, SiO2), приведенные в таблице растворимости со знаком Н, а также соли и основания. Нерастворимы в воде жидкие и твердые алканы и циклоалканы.
К малорастворимым в воде (в таблице растворимости отмечены М) относятся твердые вещества: Ca(OH)2, LiF, BaF2, MgCO3, Li3PO4, жидкие: бензол, толуол, CCl4, CHCl3, CH2Cl2, газы: Ar, Kr, Xe, O2, NO, N2O, газообразные алканы и алкены.
Растворимыми в воде веществами (в таблице растворимости отмечены Р) являются:
Растворяя вещество в воде, можно получить насыщенные и ненасыщенные растворы.
Насыщенным называют такой раствор, в котором при заданной температуре вещество больше не растворяется. Соответственно, в ненасыщенном растворе можно растворить дополнительное количество вещества.
Именно к насыщенным растворам относится количественная характеристика способности вещества к растворению, или растворимость. Растворимость измеряют, определяя содержание растворенного вещества в его насыщенном растворе при заданной температуре.
Наиболее часто используют численную характеристику — растворимость (s). Растворимость численно равна максимальной массе вещества, способного при данной температуре раствориться в 100 г растворителя. Так, s10(KNO3) равна 21 г/100 г воды при 10 °С.
Растворимость газа определяют как максимальный объем газа (V, см3), растворяющегося в 100 г растворителя при заданных температуре и давлении. Часто используют такую единицу измерения, как количество объемов растворенного газа на один объем воды.
Растворимость нередко измеряют и в других величинах, указывая массовую долю или молярную концентрацию растворенного вещества в насыщенном растворе. Эти же величины применяют для количественного выражения состава ненасыщенных растворов. К этим величинам вы обратитесь, изучая материал следующего параграфа.
Как вам уже известно, вещества по растворимости в воде условно делят на три группы (см. второй форзац). Вещество считают растворимым, если при 20 °С растворяется более 1 г вещества в 100 г воды или 100 см3 в 100 г воды в случае газов. Вещество малорастворимо, если его растворимость находится в пределах от 0,01 до 1 г в 100 г воды, и практически нерастворимо при растворимости менее 0,01 г в 100 г воды.
Концентрированные растворы содержат много растворенного вещества, а в разбавленных растворах концентрация растворенного вещества мала. Деление растворов на концентрированные и разбавленные условно. Оно не связано с делением на насыщенные и ненасыщенные растворы. Например, насыщенный раствор BaSO4 содержит 0,0002448 г соли на 100 г воды при 20 °С. Значит, это очень разбавленный раствор. Насыщенный раствор KOH содержит 112 г/100 г воды. Если растворить 80 г KOH в 100 г воды, то получим концентрированный, но ненасыщенный раствор.
Растворимость твердых и жидких веществ зависит от их природы и температуры раствора. С увеличением температуры растворимость большинства твердых веществ и жидкостей заметно возрастает (рис. 51). При охлаждении, соответственно, растворимость уменьшается и часть вещества выпадает в виде осадка — кристаллизуется.
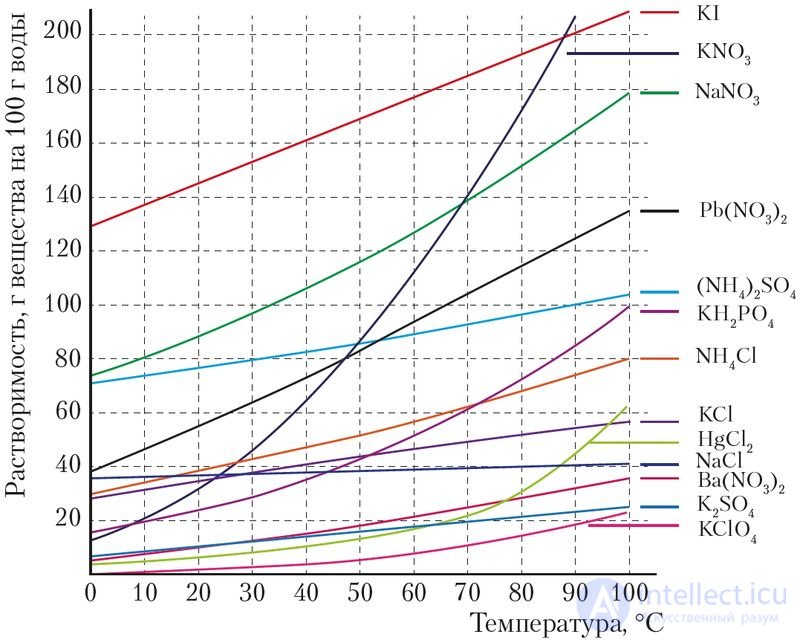
Рис. 51. Зависимость растворимости твердых веществ от температуры
Кристаллизация играет огромную роль в природе: она приводит к образованию многих минералов, например галита (NaCl), сильвина (KCl), сталактитов и сталагмитов (СаСО3). В промышленности методом кристаллизации выращивают крупные кристаллы NaCl, LiF для оптических приборов, кристаллы SiO2 для ультразвуковых генераторов, микрофонов и др.
Растворимость газов в воде зависит от их природы, температуры и давления (рис. 52, 53).
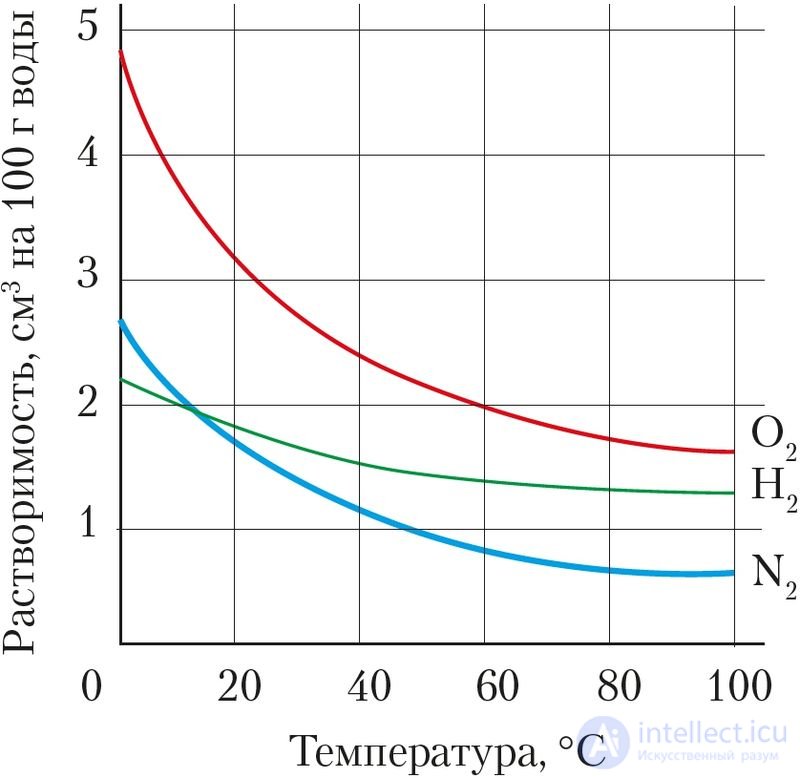
Рис. 52. Зависимость растворимости
газообразных веществ в воде
от температуры
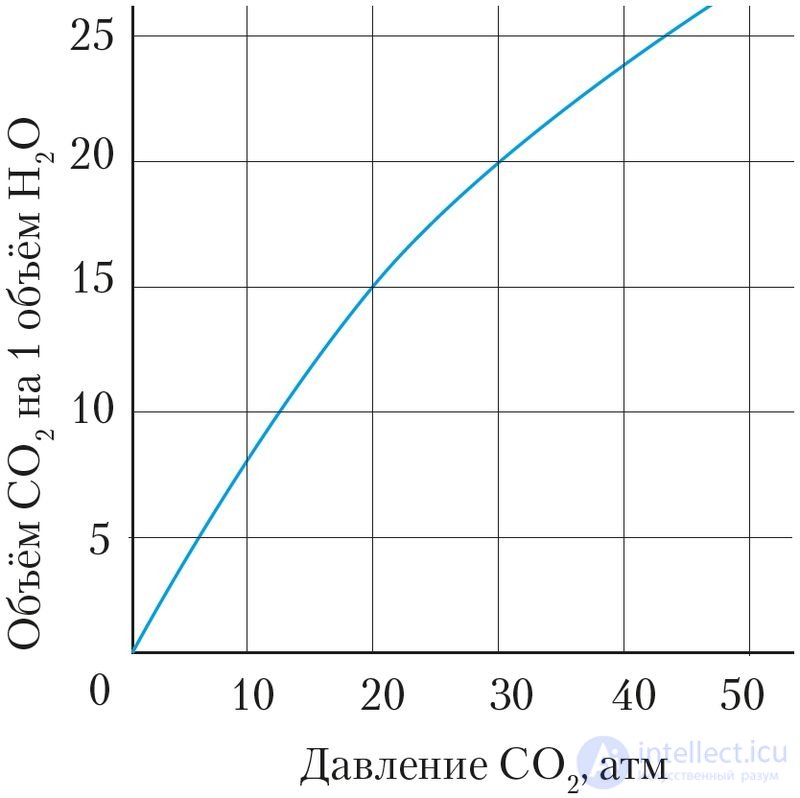
Рис. 53. Зависимость растворимости
углекислого газа в воде от давления
При растворении газов выделяется теплота. При повышении температуры их растворимость понижается. При увеличении давления растворимость газа повышается. Поэтому, указывая растворимость газа в воде при заданной температуре, имеют в виду растворимость при его давлении 1 атм или 101,325 кПа.
Некоторые жидкости, такие как H2SO4, HNO3, HF (tкип. = 19,5 °C), CH3COOH, HCOOH, CH3OH, C2H5OH, этиленгликоль, глицерин, ацетон, смешиваются с водой в любых соотношениях, поэтому говорят об их неограниченной растворимости.

Рис. 53.1. Кристалл медного купороса CuSO4 · 5H2O в его насыщенном растворе
По кривым растворимости, примеры которых представлены на рисунках 51−53, можно провести различные расчеты. Так, можно определить массу вещества, которое выпадает в осадок из насыщенного раствора при его охлаждении. Например, по кривой растворимости видно, что если приготовить насыщенный при 70 °C раствор нитрата калия в 100 г воды, а затем охладить этот раствор до 30 °С, то из него выпадет соль массой 140 – 50 = 90 г.
Повторная кристаллизация соединений из их насыщенного раствора путем его охлаждения или упаривания части растворителя называется перекристаллизацией и лежит в основе метода очистки твердых веществ. В процессе перекристаллизации растворимые примеси обычно остаются в растворе и в осадок не выпадают, поскольку образуют ненасыщенный раствор.
Если в насыщенный раствор вещества поместить его маленький кристаллик, то по мере испарения растворителя на поверхности этого кристаллика будет осаждаться растворенное вещество и образуется большой однородный кристалл (рис. 53.1).
В ряде случаев в результате физико-химического взаимодействия частиц растворенного вещества с водой образуются соединения — гидраты. Такой процесс называют гидратацией. Молекулы воды при этом не разрушаются, а связываются с молекулами или ионами растворенного вещества.
Гидраты — это продукты присоединения воды к неорганическим и органическим веществам, в которых молекула воды присутствует в виде отдельной структурной единицы.
Многие гидраты легко распадаются, хотя могут образовывать и устойчивые соединения. В ряде случаев после упаривания растворителя и кристаллизации растворенного соединения можно выделить кристаллогидраты.
Большинство кристаллогидратов являются солями. Кристаллогидраты образуются, если в кристаллической решетке катионы связываются с молекулами воды более прочно, чем с анионами в кристаллах безводной соли. Состав кристаллогидрата выражают формулой, указывающей число молекул кристаллизационной воды на одну структурную единицу вещества, например кристаллическая сода Na2CO3 · 10H2O, гипс CaSO4 · 2H2O, медный купорос CuSO4 · 5H2O. С этими кристаллогидратами вы уже знакомы из курсов химии 8-го и 9-го классов.
Иногда кристаллогидраты образуют кислоты (щавелевая, лимонная), основания (KOH · 2H2O, NaOH · H2O, Ba(OH)2 · 8H2O), а также некоторые углеводы (глюкоза) и их производные (сорбит).
Кристаллогидраты — это кристаллические продукты присоединения воды к неорганическим и органическим веществам, имеющие определенный состав и включающие молекулы воды в виде отдельной структурной единицы. Вода, входящая в состав кристаллогидратов, называется кристаллизационной.
Многие кристаллогидраты ярко окрашены. Например, безводный CoCl2 имеет синий цвет. В результате гидратации он превращается в темно-розовый кристаллогидрат CoCl2 · 6H2O (рис. 54, а) и поэтому может использоваться в качестве индикатора присутствия воды. Аналогичную роль может играть и сульфат меди(II): безводный CuSO4 — бледно-голубой, кристаллогидрат CuSO4 · 5H2O — ярко-синий (рис. 54, б).

Рис. 54. Безводные соли и кристаллогидраты
Процесс образования кристаллогидратов используется в строительстве. Так, порошок цемента в основном состоит из смеси безводных кристаллов 3CaO · SiO2 и 2CaO · SiO2. При смешивании цемента с водой протекают процессы гидратации и образования кристаллогидратов 3CaO · SiO2 · 3H2O и 2CaO · SiO2 · 3H2O. При этом пластичный цементный клей, напоминающий по консистенции тесто, затвердевает и превращается в цементный камень.
Молекулы воды в гидратах связываются с молекулами или ионами растворенного вещества за счет донорно-акцепторного, электростатического взаимодействия или образования водородных связей.
В гидратах молекулы или ионы растворенного вещества оказываются окруженными более или менее тесно связанными с ними молекулами воды, число которых может меняться.
Гидратную теорию растворов предложил Д. И. Менделеев. Он писал: «Растворы суть химические соединения, определяемые силами, действующими между растворителем и растворенным телом».
Тот факт, что образование растворов в значительной степени является химическим взаимодействием, подтверждается не только выделением или поглощением теплоты при растворении, но и уменьшением объема раствора в сравнении с исходным суммарным объемом его компонентов. Например, при смешивании 50 мл этанола с 50 мл воды образуется 97 мл раствора. Раствор при этом немного нагревается.
В таблице 15.1 приведены примеры наиболее распространенных кристаллогидратов.
Таблица 15.1. Формулы, внешний вид и названия кристаллогидратов
| Название кристаллогидрата | Химическая формула | Внешний вид |
|---|---|---|
| Кристаллическая сода, декагидрат карбоната натрия | Na2CO3 · 10H2O |
|
| Медный купорос, пентагидрат сульфата меди(II) | CuSO4 · 5H2O |
|
| Железный купорос, гептагидрат сульфата железа(II) | FeSO4 · 7H2O |
|
| Цинковый купорос, гептагидрат сульфата цинка(II) | ZnSO4 · 7H2O |
|
| Глауберова соль, декагидрат сульфата натрия | Na2SO4 · 10H2O |
|
| Гипс, дигидрат сульфата кальция | CaSO4 · 2H2O |
|
Растворы — гомогенные устойчивые системы переменного состава, состоящие из нескольких компонентов.
Растворение — это физико-химический процесс, сопровождающийся выделением или поглощением теплоты.
Растворимость веществ зависит от их природы и температуры. На растворимость газов влияет давление.
Кристаллогидраты — это кристаллические продукты присоединения воды к неорганическим и органическим веществам, имеющие определенный состав и включающие молекулы воды в виде отдельной структурной единицы.
1. Приведите примеры твердых, жидких и газообразных растворов. Укажите области применения твердых растворов.
2. Укажите основные различия между раствором и механической смесью веществ.
3. Пользуясь данными таблицы растворимости на форзаце учебника, приведите по два примера:
Запишите их формулы.
4. Даны соединения: хлороводород, нитрат калия, хлорид калия, хлорид натрия, оксид серы(IV), аммиак. С помощью кривых растворимости (рис. 51), а также знаний о растворимости газов определите вещества, растворимость которых в воде при повышении температуры:
5. Назовите процессы взаимодействия между молекулами воды и растворяемым веществом при образовании водного раствора.
6. По кривым растворимости (рис. 51) найдите растворимость солей: нитрата натрия, хлорида аммония и хлорида натрия при 20 °С, 50 °С, 70 °С.
7. Растворимость натриевой селитры NaNO3 при 10 °С равна 80 г на 100 г воды. Определите массовую долю соли в насыщенном растворе при этой температуре.
8. Массовая доля KNO3 в насыщенном при 20 °С растворе равна 24,0 %. Определите растворимость KNO3 при 20 °С (г/100 г воды).
9. Рассчитайте, на сколько граммов различается масса 500 г безводного сульфата кальция и его двухводного кристаллогидрата (гипса).
10. Растворимость аммиака при 0 °С равна 1153 объема на 1 объем воды, а при 30 °С — 532 объема (при н. у.) на 1 объем воды. Насыщенный при 0 °С раствор массой 250 г нагрели до 30 °С. Как изменилась его масса? Какой объем (при н. у.) аммиака выделился при нагревании? Ответ подтвердите расчетом.
1. Процесс растворения NaCl в воде сопровождается:
2. Декагидрату сульфата натрия соответствует формула:
3. К раствору относятся системы:
4. Растворимость газа в воде можно увеличить:
5. Растворимость нитрата калия s10(KNO3) = 60 г/100 г воды. Его раствор с массовой долей 0,375 является:
Исследование, описанное в статье про растворение, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое растворение и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия