Лекция
Привет, Вы узнаете о том , что такое неметаллы , Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое неметаллы , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Изучив эту главу, вы расширите и систематизируете сведения о неметаллах на основании знаний о строении атомов, химической связи и строении вещества. Каждый из представленных неметаллов вы будете рассматривать как химический элемент и как простое вещество, изучите особенности важнейших соединений неметаллов (оксидов, гидроксидов, солей и водородных соединений).
Характеристики химических элементов даны по плану, предложенному в главе «Строение атома и периодический закон», в который дополнительно включены вопросы распространенности элемента в природе и его биологической роли.
В характеристиках веществ рассмотрены их состав и строение, физические и химические свойства, способы получения в лаборатории и промышленности, области практического использования.
Важнейшие понятия темы:
неметаллы , кислотные оксиды, кислоты, соли, аммиак, строительные материалы, качественные реакции на ионы ,
,
,
,
,
Химические элементы принято делить на металлы и неметаллы по их химическим свойствам. В периодической системе неметаллы расположены в А-группах: IА, IIIА–VIIIА. От металлов их отделяет ступенчатая линия водород — бор — оганесон. Неметаллы находятся выше этой линии, то есть занимают правый верхний угол таблицы, образуя своеобразный треугольник (рис. 61).
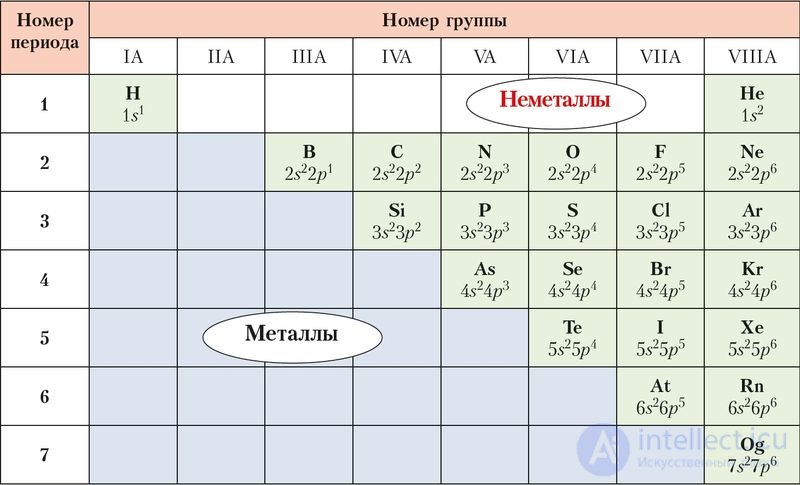
Рис. 61. Неметаллы и электронная конфигурация их внешнего энергетического уровня
Элементы, расположенные в одной группе, сходны по строению атома, а значит, во многом и по свойствам. Поэтому для некоторых групп неметаллов применяют общие названия. Так, неметаллы VIIIA-группы называют благородными газами. Для элементов VIIA-группы используют название галогены — рождающие соли. Неметаллы VIA-группы имеют общее название халькогены — рождающие руды.
По электрофизическим свойствам, в отличие от химических, простые вещества, состоящие из атомов тех или иных элементов, подразделяют на три группы: металлы, полупроводники и диэлектрики. Различить эти вещества можно не только по величине электропроводности, но и по характеру ее зависимости от температуры. С ростом температуры электропроводность металлов падает, а полупроводников и диэлектриков растет. Типичные полупроводники — кремний и германий.
Внешний электронный слой атома во многом определяет свойства элемента. Число электронов внешнего уровня атомов неметаллов соответствует номеру А-группы, в которой расположен элемент. У большинства из них он близок к завершению или завершен, содержит четыре и более электронов. Меньшее число электронов содержат атомы лишь трех элементов: водород имеет один электрон (до завершения не хватает одного электрона), гелий — два электрона (внешний уровень завершен), бор — три электрона. Неметаллы являются представителями p-элементов, за исключением водорода и гелия, принадлежащих к s-элементам.
Атомы неметаллов, в отличие от атомов металлов, способны проявлять как положительные степени окисления, так и отрицательные. Исключением являются фтор и благородные газы. В соединениях с другими элементами для фтора характерна лишь отрицательная степень окисления, равная –1 (например, ,
,
). Наиболее легкие благородные газы — гелий, неон и аргон — устойчивых соединений не образуют, а для ксенона, криптона и радона получены соединения лишь с положительными степенями окисления (например,
,
).
В целом значения степеней окисления неметаллов лежат в интервале от –4 до +8, а валентности — от I до VIII. Следует вспомнить, что валентность атомов элементов второго периода не бывает больше четырех:

В исторически сложившейся классификации элементов принадлежность к неметаллам определяли по физическим свойствам простых веществ: твердое, газообразное или жидкое состояние при нормальных условиях. Об этом говорит сайт https://intellect.icu . В твердом состоянии у неметаллов, как правило, отсутствует металлический блеск. Их электро- и теплопроводность обычно невелики, вещества являются хрупкими.
Неметаллы образуют два типа кристаллов — молекулярные и атомные (рис. 62).

Рис. 62. Состав и строение простых веществ неметаллов
Вещества молекулярного строения отличаются низкими температурами плавления (гелий –272 °С, кислород –223 °С) и кипения (гелий –269 °С, кислород –183 °С). Неметаллы немолекулярного строения, наоборот, имеют чрезвычайно высокие температуры кипения и плавления (графит: Tпл. = 3850 °С, Tкип.= 4200 °С).
Для неметаллов характерно явление аллотропии. Примерами могут служить красный и белый фосфор, алмаз и графит, кислород и озон.
Неметаллы могут вступать в реакции с веществами всех классов (металлами, другими неметаллами, оксидами, щелочами, кислотами, солями) и проявлять как окислительные, так и восстановительные свойства (табл. 20).
Таблица 20. Общие свойства неметаллов как простых веществ
| Неметаллы как окислители вступают в реакции | Неметаллы как восстановители вступают в реакции |
| С металлами: |
С некоторыми оксидами: |
| С другими неметаллами: |
С другими неметаллами: |
| С кислотами: |
С органическими веществами: |
| С солями: |
Окислительные способности атомов неметаллов можно сравнивать по положению в периодической системе: с ростом атомного номера они увеличиваются в периодах и уменьшаются, как правило, в группах. Эти же свойства можно также оценивать, сопоставляя электроотрицательность неметаллов, которая возрастает в ряду:
| Si | B | As | As | H | C | I | S | Br | Cl | N | O | F |
| 1,9 | 2,0 | 2,1 | 2,2 | 2,2 | 2,5 | 2,5 | 2,6 | 2,8 | 3,0 | 3,0 | 3,5 | 4,0 |
 |
||||||||||||
Окислительная способность неметаллов с увеличением электроотрицательности усиливается.
В природе неметаллы существуют не только в виде соединений (органические вещества, оксиды Н2О, SiO2, СО2, соли бескислородных кислот NaCl, As2S3, соли кислородсодержащих кислот СаСО3, Са3(РО4)2), но и в свободном виде, например азот, кислород, благородные газы, углерод (в форме графита и алмаза), сера. Существование неметаллов в виде простых веществ в природе связано с низкой активностью перечисленных неметаллов при нормальных условиях: атомы благородных газов имеют завершенный внешний электронный уровень, кислород и азот — достаточно прочные ковалентные связи в двухатомных молекулах, углерод образует прочные атомные кристаллы. На Земле самыми распространенными неметаллами являются кислород и кремний (по массе около 49 % и 26 % соответственно), во Вселенной — водород.
Области применения простых веществ неметаллов обширны. Примерами могут служить: производство полупроводниковых материалов (кремний, селен), металлургические процессы получения металлов (углерод, водород) и сплавов (бор, кремний), интенсификация процессов горения (кислород), создание инертной атмосферы (азот, благородные газы), органический синтез (хлор, бром), воздухоплавание (гелий, водород), светотехника (благородные газы).
Неметаллы являются представителями s- и р-элементов.
Степени окисления неметаллов изменяются от –4 до +8.
В химических реакциях неметаллы проявляют как окислительные, так и восстановительные свойства.
1. Опишите положение неметаллов в периодической системе. Укажите для элементов-неметаллов третьего периода возможные значения степени окисления и валентности.
2. Запишите символы элементов и общую формулу электронной конфигурации:
3. Определите степени окисления атомов в соединениях:
4. Укажите утверждения, характеризующие кислород как химический элемент:
5. Составьте уравнения реакций с участием неметаллов, учитывая, что атомы неметаллов в заданных реакциях проявляют низшую степень окисления:
6. Определите массу углерода, необходимого для восстановления железа из оксида железа(III) массой 1 т. Углерод окисляется до высшей степени окисления.
7. Азот имеет очень низкие температуры плавления и кипения –210 °C и –196 °C, а бор высокие — ≈2075 °C и ≈3800 °C соответственно. Дайте объяснение такому различию.
8. Докажите, что фосфор выполняет функцию восстановителя в первой реакции и окислителя — во второй:
9. Расставьте коэффициенты методом электронного баланса и укажите, окислителем или восстановителем являются простые вещества:
10. Образец газообразного простого вещества неметалла объемом 1 дм3 (н. у.) имеет массу 3,17 г. Определите химическую формулу вещества.
1. Конфигурацию внешнего электронного уровня ns2np5 имеют:
2. Кремний как химический элемент характеризуют утверждения:
3. Положительную степень окисления проявляют элементы VA-группы в соединениях:
4. Сера является окислителем, реагируя с:
5. Сумма коэффициентов в реакции синтеза фосфида кальция из простых веществ равна:
Исследование, описанное в статье про неметаллы , подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое неметаллы и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия