Лекция
Привет, Вы узнаете о том , что такое оксиды азота, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое оксиды азота , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Азот образует с кислородом ряд оксидов: ,
,
,
,
. Два из этих оксидов — N2O, NO — относятся к несолеобразующим, остальные — к кислотным.
Оксид азота(II) NO в обычных условиях представляет собой бесцветный газ (tкип. = −151,7 °С, tпл. = −163,7 °С).
В природе он образуется в результате взаимодействия простых веществ при грозовых разрядах (около 3000 °С):
N2 + O2 2NO – Q,
в промышленности — как промежуточный продукт превращения аммиака в азотную кислоту:
4NH3 + 5O2 4NО + 6H2O.
В лаборатории его получают действием разбавленной азотной кислоты на медь:
3Cu + 8HNO3(разб) = 3Cu(NO3)2 + 2NO↑ + 4H2O.
Оксид азота(II) образуется при работе двигателей внутреннего сгорания из азота и кислорода под действием высокой температуры и давления.
Оксид азота(II) не реагирует ни с кислотами, ни со щелочами. Однако легко вступает в окислительно-восстановительные реакции. Так, оксид азота(II) быстро окисляется кислородом с образованием оксида азота(IV):
.
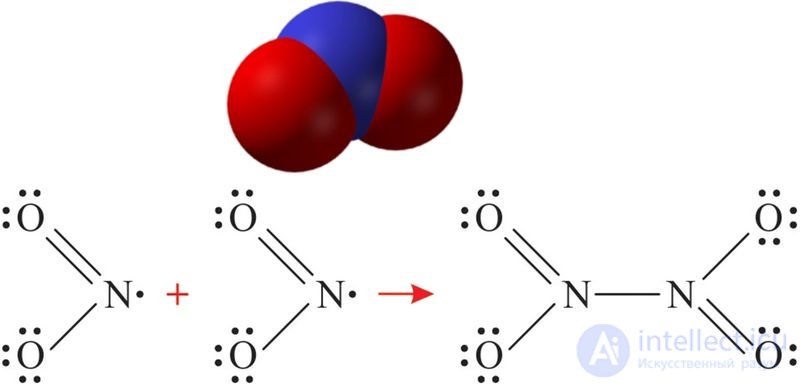
Рис. 94.1. Масштабная модель молекулы оксида азота(IV); строение молекул NO2 и их димеризация с образованием N2O4
Оксид азота(IV). Получение и химические свойства
Молекула NO2 имеет угловую форму (рис. Об этом говорит сайт https://intellect.icu . 94.1). Предполагается, что атом азота находится в состоянии sp2-гибридизации, длина связи N—O равна 0,119 нм, что соответствует полуторной связи.
Оксид азота(IV) NO2, диоксид азота — газ бурого цвета (tпл. = −11,2 °С, tкип. = 21 °С), в жидком и твердом состоянии бесцветен и состоит из молекул N2O4 вследствие димеризации:
2NO2 N2O4 + Q.
Димеризация легко происходит из-за наличия неспаренного электрона. В газообразном состоянии оксид азота(IV) димеризован частично.
В лаборатории обычно его получают известной вам реакцией концентрированной азотной кислоты с медью:
Cu + 4HNO3(конц) = Cu(NO3)2 + 2NO2↑ + 2H2O
или разложением некоторых нитратов (§ 38, с. 211).
Оксид азота(IV) взаимодействует с водой. В зависимости от условий образуются различные продукты. Так, при комнатной температуре образуются азотная и азотистая кислоты:
.
При растворении NO2 в воде при повышенной температуре в избытке кислорода образуется азотная кислота:
.
Равновесие этой обратимой реакции при промышленном получении азотной кислоты смещают вправо, повышая давление.
При растворении NO2 в щелочах образуются нитраты вместе с нитритами:
Недостаточная очистка газов, выделяемых в окружающую среду предприятиями, производящими азотную кислоту, котлами электростанций, газотурбинными установками, двигателями автомобилей и самолетов, приводит к загрязнению атмосферы оксидами азота. Под действием кислорода NO превращается в NO2. Во влажной атмосфере образуется азотная кислота, и на землю выпадают кислотные дожди, вредные не только для человека и животных, но и для растений. Под действием кислотных дождей разрушаются строительные сооружения.
Газообразный оксид азота(I) N2O при вдыхании приводит к снижению болевой чувствительности, поэтому его иногда применяют в смеси с кислородом для наркоза.
Оксид N2O3 устойчив только при низких температурах (tпл. −102 °С, tкип. 4 °С, tразл. 4,5 °С) и представляет собой жидкость голубого цвета. При взаимодействии с водой образует азотистую кислоту:
.
Оксид азота(V) N2O5 — твердое вещество белого цвета. Реагируя с водой, образует азотную кислоту:
.
Оксид азота(II) — несолеобразующий оксид. При взаимодействии с кислородом превращается в оксид азота(IV).
Оксид азота(IV) проявляет окислительные свойства; при растворении в воде в присутствии кислорода образует азотную кислоту.
1. Выпишите формулы солеобразующих оксидов: N2O5, NO2, N2O3, NO, N2O.
2. Запишите формулы оксидов, которые соответствуют кислотам HNO2 и HNO3.
3. Какие из оксидов азота можно собирать методом вытеснения воды?
4. Какие из оксидов азота могут реагировать со щелочами? Запишите формулы этих оксидов.
5. Запишите уравнения реакций, соответствующих взаимодействию оксида азота(IV) с водой в различных условиях.
6. Определите сумму электронов в молекуле: а) оксида азота(II); б) оксида азота(IV).
7. Укажите, в какую сторону сместится равновесие в реакции 2NO2(г) N2O4(г) + Q:
Как изменяется окраска реакционной смеси в каждом случае?
8. Расставьте коэффициенты методом электронного баланса:
NaOH + O2 + NO2 = NaNO3 + H2O.
9. Составьте уравнения реакций согласно схеме:
.
10. Определите массовую долю (%) соли, которая образовалась в растворе при пропускании оксида азота(IV) объемом 1,12 дм3 (н. у.) в смеси с избытком кислорода через раствор гидроксида кальция массой 300 г с массовой долей щелочи 0,166 %.
1. Несолеобразующими оксидами являются:
2. Как окислителем, так и восстановителем в химических реакциях могут быть:
3. Продуктами взаимодействия NO2 с водой могут быть:
4. Оксид азота NO2 образует соли, реагируя с:
5. Объем газа (н. у.), полученного в реакции меди массой 3,2 г с концентрированной азотной кислотой при выходе продукта 85 %, равен:
Исследование, описанное в статье про оксиды азота, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое оксиды азота и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Из статьи мы узнали кратко, но содержательно про оксиды азотаОтветы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии