Лекция
Привет, Вы узнаете о том , что такое реакции ионного обмена, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое реакции ионного обмена , настоятельно рекомендую прочитать все из категории Неорганическая химия.
. Об этом говорит сайт https://intellect.icuРеактивы: растворы гидроксида натрия, серной кислоты, хлорида натрия, карбоната натрия, хлорида железа(III), нитрата калия, фенолфталеина.
Проведите реакции между следующими парами веществ:
Составьте уравнения проведенных реакций в молекулярной форме, полной и сокращенной ионной формах. Укажите, какие эффекты вы наблюдали.
Сделайте вывод о необходимых условиях протекания реакций ионного обмена.
реакции ионного обмена — это химические процессы в растворах электролитов, при которых вещества обмениваются ионами. Они протекают только тогда, когда в результате образуется осадок, газ или слабый электролит (например, вода). В противном случае реакции обмена являются обратимыми.
Реакция ионного обмена — взаимодействие между растворами кислот, оснований и солей, при котором ионы меняются местами.
Важная особенность: степень окисления элементов не изменяется, так как это не реакции окислительно-восстановительные, а чисто обменные.
Чтобы реакция прошла, необходимо выполнение хотя бы одного условия:
Образование осадка (например, Fe(OH)₃).
Выделение газа (например, CO₂ при взаимодействии карбонатов с кислотами).
Образование слабого электролита (например, H₂O при нейтрализации кислоты и основания).
Если ни одно из условий не выполняется (например, смешивание растворов NaCl и KNO₃), реакция не идет.
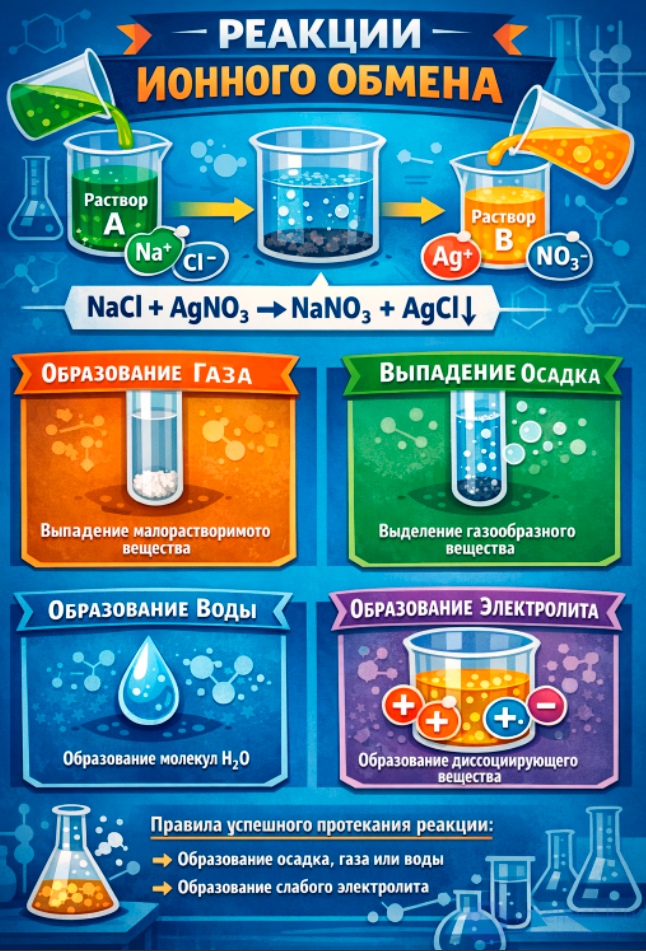
Реакции ионного обмена принято записывать в трех формах:
Молекулярная форма — показывает вещества целиком. Пример:
Полная ионная форма — все сильные электролиты расписываются на ионы.
Сокращенная ионная форма — остаются только те частицы, которые реально участвуют в реакции.

Выпадение осадка (бурый Fe(OH)₃).
Выделение газа (CO₂).
Изменение цвета индикатора (фенолфталеин обесцвечивается при нейтрализации).
Растворение осадка при взаимодействии с кислотой.
Молекулярное уравнение:
Полное ионное уравнение:
Сокращенное ионное уравнение:
Наблюдение: фенолфталеин обесцвечивается (щелочная среда → нейтрализация).
Молекулярное уравнение:
Полное ионное уравнение:
Сокращенное ионное уравнение:
Наблюдение: бурый студенистый осадок гидроксида железа(III).
Молекулярное уравнение:
Полное ионное уравнение:
Сокращенное ионное уравнение:
Наблюдение: выделение пузырьков газа (углекислый газ).
Молекулярное уравнение:
Ионное уравнение: отсутствует, так как нет осадка, газа или слабого электролита.
Наблюдение: изменений не происходит.
Молекулярное уравнение:
Полное ионное уравнение:
Сокращенное ионное уравнение:
Наблюдение: бурый осадок растворяется, образуется прозрачный раствор соли.
Реакции ионного обмена протекают при выполнении одного из условий:
образование осадка (Fe(OH)₃);
выделение газа (CO₂);
образование слабого электролита (H₂O).
Если ни одно из условий не выполняется (пример: KNO₃ + NaCl), реакция не идет.
Исследование, описанное в статье про реакции ионного обмена, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое реакции ионного обмена и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Из статьи мы узнали кратко, но содержательно про реакции ионного обмена
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия