Лекция
Привет, Вы узнаете о том , что такое 1.3. Основные классы неорганических соединений, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое 1.3. Основные классы неорганических соединений , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Изучаемые вещества классифицируют с учетом состава, строения, свойств и других критериев. Основными классами простых веществ являются металлы и неметаллы, сложных — оксиды, кислоты, основания и соли. Их состав, свойства и способы получения вы изучали ранее. В данном параграфе вспомним принципы номенклатуры и классификации веществ (рис. 6).
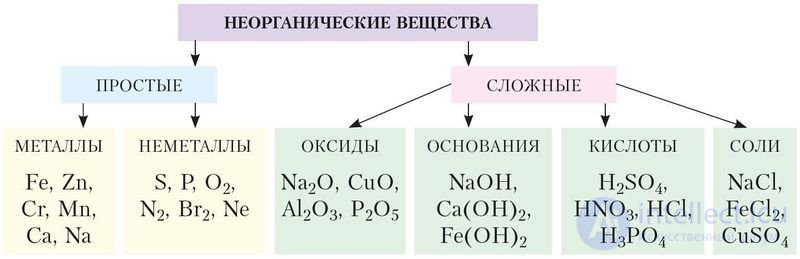
Рис. 6. Классы неорганических веществ

Неорганические вещества принято делить на классы (рис. 6.1). В каждом из классов объединяют вещества, сходные по составу, строению, свойствам. Согласно одной из общепринятых классификаций, различают простые (металлы и неметаллы) и сложные вещества. Важнейшими классами сложных неорганических веществ являются оксиды, кислоты, основания и соли. Как вам известно, основания и кислородсодержащие кислоты имеют общее название — гидроксиды.

Рис. 6.1. Важнейшие классы неорганических соединений





Металлы — простые твердые при комнатной температуре вещества (за исключением жидкой ртути), обладающие пластичностью и теплопроводностью, высокой электропроводностью. Полированные поверхности металлов всегда блестящие.
Неметаллы — простые твердые, жидкие или газообразные при комнатной температуре вещества. В твердом состоянии они, как правило, непластичные или даже хрупкие, плохо проводят тепло и электрический ток.
Оксиды — сложные вещества, состоящие из двух элементов, один из которых кислород (ЭхОу).
Оксиды металлов при нормальных условиях — твердые вещества. Оксиды неметаллов при этих же условиях могут быть в твердом, жидком и газообразном состояниях.
Кислород в оксидах проявляет степень окисления –2: (оксид углерода(IV),
(оксид кальция).

Напомним: если атомы элемента могут существовать в разных положительных степенях окисления, эту степень в названиях или формулах оксидов, оснований, солей указывают римскими цифрами. Их ставят в скобках после названия соответствующего элемента, например: оксид железа(III), гидроксид железа(II), хлорид железа(II).
Различают солеобразующие (кислотные, амфотерные, осно́вные) и несолеобразующие оксиды (рис. 7).

Рис. 7. Классификация оксидов
К кислотным относятся оксиды, которым соответствуют кислоты. Кислотные оксиды реагируют со щелочами с образованием соли и воды:
Кислотным оксидам соответствуют кислородсодержащие кислоты: оксиду соответствует кислота
(степени окисления углерода одинаковы в оксиде и кислоте).
К осно́вным относятся оксиды, которым соответствуют основания. Основные оксиды реагируют с кислотами с образованием соли и воды:
Основным оксидам соответствуют основания. Например, оксиду соответствует основание
.
Амфотерные оксиды реагируют и с кислотами, и со щелочами:
(при сплавлении).
Реакции амфотерных оксидов со щелочами могут протекать не только при сплавлении, но и в растворе:
Соединение относят к классу комплексных соединений. Дополнительные сведения о таких соединениях приведены в конце данного параграфа, а также в материале о свойствах амфотерных оксидов и гидроксидов в главе II и металлов в главе VII.
К несолеобразующим оксидам относят При комнатной температуре они не реагируют ни с кислотами, ни со щелочами.
Кислотами называют сложные вещества, содержащие атомы водорода и кислотные остатки, причем атомы водорода способны замещаться атомами металлов.
Кислоты также определяют как электролиты, при диссоциации которых в водных растворах в качестве катионов образуются только катионы водорода H+:
В таблицах 1 и 2 приведен состав и дана классификация кислот по различным признакам.
Таблица 1. Об этом говорит сайт https://intellect.icu . Названия некоторых кислот и их солей
| Бескислородные кислоты | Кислородсодержащие кислоты(гидроксиды) | ||||
| Химическая формула | Название кислоты | Название соли | Химическая формула | Название кислоты | Название соли |
| HI | Йодоводородная | Йодид | HNO3 | Азотная | Нитрат |
| HBr | Бромоводородная | Бромид | HNO2 | Азотистая | Нитрит |
| HCl | Хлороводородная | Хлорид | Н2SO4 | Серная | Сульфат |
| HF | Фтороводородная | Фторид | H2SO3 | Сернистая | Сульфит |
| H2S | Сероводородная | Сульфид | H3PO4 | Фосфорная | Фосфат |
| H2CO3 | Угольная | Карбонат | |||
| Н2SiO3 | Кремниевая | Силикат | |||
| НСlO4 | Хлорная | Хлорная | |||
Таблица 2. Классификация кислот
| Признак классификации | Классификационные группы | Примеры |
| По происхождению | Неорганические (минеральные) | НCl, H2SO4, HNO3 |
| Органические (карбоновые) | HCOOH, CH3COOH, C17H35COOH | |
| По наличию атомов кислорода | Кислородсодержащие | H3PO4, H2SO4, H2CO3 |
| Бескислородные | HCl, H2S, HF | |
| По числу атомов водорода, способных замещаться атомами металлов | Одноосно́вные | HNO3, HF, НCl, CH3COOH |
| Многоосно́вные (двухосно́вные, трехосно́вные) | H2SO4, H2SO3, H2CO3, H3PO4 | |
| По силе (способности диссоциировать на ионы в водном растворе) | Сильные | H2SO4, HNO3, НCl, HClO4 |
| Слабые | H2S, H2SiO3, CH3COOH |
Основания — сложные вещества, состоящие из атомов металлов и гидроксогрупп ОН: гидроксид натрия NaOH, гидроксид железа(II) Fe(OH)2.
Основания — это электролиты, при диссоциации которых в качестве анионов образуются только гидроксид-ионы ОН–:
Все основания реагируют с кислотами, образуя соль и воду (реакция нейтрализации):
В основе классификации оснований лежат следующие признаки.
1. Число групп ОН. По числу групп ОН, приходящихся на один атом металла, различают однокислотные (NaOH, KOH, LiOH) и многокислотные (Mg(OH)2, Ca(OH)2, Fe(OH)2) основания.
2. Растворимость в воде. Гидроксиды металлов — твердые вещества. Водный раствор аммиака — гидрат аммиака (NH3 · H2O) — также обладает основными свойствами и диссоциирует с образованием гидроксид-ионов. Для того чтобы подчеркнуть это свойство, формулу гидрата аммиака часто записывают в привычном для оснований виде — NH4OH. По растворимости в воде неорганические основания делят на растворимые (щелочи) и нерастворимые.
Щелочи — это растворимые в воде основания. К щелочам относят растворимые гидроксиды всех элементов IА-группы и щелочноземельных металлов: стронция, бария, радия, включая малорастворимый гидроксид кальция.
Амфотерные гидроксиды Zn(OH)2, Be(OH)2, Al(OH)3, подобно соответствующим им оксидам, реагируют как с кислотами, так и со щелочами. Взаимодействие со щелочами возможно в расплавах и растворах:
(сплавление);
(раствор).
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
С точки зрения теории электролитической диссоциации солями называют сложные вещества, при диссоциации которых образуются катионы металлов и анионы кислотных остатков:
К солям относят также соединения, содержащие ион аммония и кислотный остаток (хлорид аммония NH4Cl, сульфат аммония (NH4)2SO4 и др.)
В основе систематических названий солей лежат названия кислотного остатка и металла с указанием в скобках римскими цифрами степени окисления атомов металла, если она может иметь разные значения. Например, MgSO4 — сульфат магния, FeCl2 — хлорид железа(II), Fe2(SO4)3 — сульфат железа(III).
В зависимости от полноты замещения атомов водорода в кислотах различают средние и кислые соли.
Кислые соли могут образовывать многоосно́вные кислоты (Н2SO4, Н2СO3, Н2S, Н3РO4) при частичном замещении атомов водорода в их молекулах. Наличие в составе кислой соли атомов водорода отражается в названии, например NaHCO3 — гидрокарбонат натрия (питьевая сода), Са(НСО3)2 — гидрокарбонат кальция, NaH2PO4 — дигидрофосфат натрия, NaHSO4 — гидроcульфат натрия.
На следующей схеме показана возможность полного и неполного замещения.


При неполном замещении гидроксогрупп в основании на кислотные остатки образуются осно́вные соли. В качестве примера основных солей можно привести Al(OH)2NO3. Эту соль можно рассматривать как продукт замещения одной группы ОН в основании Al(OH)3 на кислотный остаток .
Отдельную группу солей образуют так называемые комплексные соединения. В курсе химии 11-го класса вы встретитесь с некоторыми из таких соединений: Na2[Zn(OH)4] — тетрагидроксоцинкат натрия, K3[Al(OH)6] — гексагидроксоалюминат калия. Они содержат комплексные ионы, которые в химических формулах заключают в квадратные скобки.
Соли, в состав которых входят молекулы воды, называют кристаллогидратами, а вода — кристаллизационной: FeSO4 · 7H2O (железный купорос, или гептагидрат сульфата железа(II)), Na2SO4 · 10H2O (глауберова соль, или декагидрат сульфата натрия).

Из курса органической химии вам известны соли карбоновых кислот (ацетат натрия СН3СООNa, стеарат калия C17H35COOK) и соли аминов (хлорид метиламмония СН3NH3Cl, гидросульфат фениламмония С6Н5NH3HSO4).
К основным классам простых неорганических веществ относят металлы и неметаллы, сложных — оксиды, основания, кислоты и соли.
Вопросы, задания, задачи
1. Заполните таблицу, используя формулы веществ: Fe(ОН)2, СаО, Н2SO4, SО3, СО2, NaOH, Na2SO4, НСl, Н2SO3, K3PO4, Ba(ОН)2, КСl.
| Оксиды | Кислоты | Основания | Соли |
2. Выпишите формулы одноосновных кислот: H3PO4, СН3СООН, НI, H2S, HNO2.
3. Составьте формулы оксидов: а) соответствующих кислотам:
| Кислота | ||||||
| Кислотный оксид |
б) соответствующих основаниям:
| Основание | LiOH | NaOH | Ba(OH)2 | Ca(OH)2 | Fe(OH)2 | Sr(OH)2 |
| Основный оксид |
4. Назовите вещества, формулы которых:
5. Составьте формулы веществ:
6. Выберите вещества, реагирующие:
Составьте уравнения соответствующих реакций.
7. Вычислите и сравните массовую долю натрия в его хлориде и сульфате.
8. Определите элемент Х и назовите соединение К3ХO4, массовая доля кислорода в котором равна 30,19 %.
9. Назовите вещества в схеме, составьте уравнения реакций согласно схеме:
10. Рассчитайте массовую долю хлора в смеси, в которой массовая доля хлорида калия составляет 67 %, хлорида натрия — 27 %, оксидов кремния и железа — 6 %.
Исследование, описанное в статье про 1.3. Основные классы неорганических соединений, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое 1.3. Основные классы неорганических соединений и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии