Лекция
Привет, Вы узнаете о том , что такое водородные соединения, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое водородные соединения , настоятельно рекомендую прочитать все из категории Неорганическая химия.
Рассмотрим изменение кислотно-основных свойств водных растворов летучих водородных соединений в зависимости от положения элемента в периодической системе. Известно, что СН4 не растворяется в воде, NH3 образует слабое основание NH3 ∙ Н2O, а раствор НF — слабая кислота:
NH3 ∙ Н2O
+ OН–;
Н2О Н+ + ОН–;
HF H+ + F–.
Значит, кислотные свойства водородных соединений неметаллов в периоде с увеличением порядкового номера элемента усиливаются.
В группах кислотные свойства водных растворов водородных соединений неметаллов также усиливаются: НF является слабой кислотой, а HCl, HBr, HI — сильными.

Углерод и водород образуют значительное число бинарных органических соединений различных классов: алканы СnH2n+2, алкены СnH2n, алкины СnH2n–2, арены СnH2n–6 и др.
Кислород образует два устойчивых соединения с водородом — Н2О и Н2О2 (вода и пероксид водорода).
Для серы известен ряд водородных соединений состава Н2Sn (n = 1–20), например, Н2S, Н2S2.
Водородные соединения щелочных и щелочноземельных металлов можно получить прямым соединением простых веществ, например:
Н2 + 2Li = 2LiH,
Н2 + Вa = ВaH2.
Для этого водород под давлением пропускают над разогретым до 200−600 °С металлом.
Наиболее распространенные соединения водорода с неметаллами, а также металлами IA- и IIA-групп представлены на рисунке 67.1.
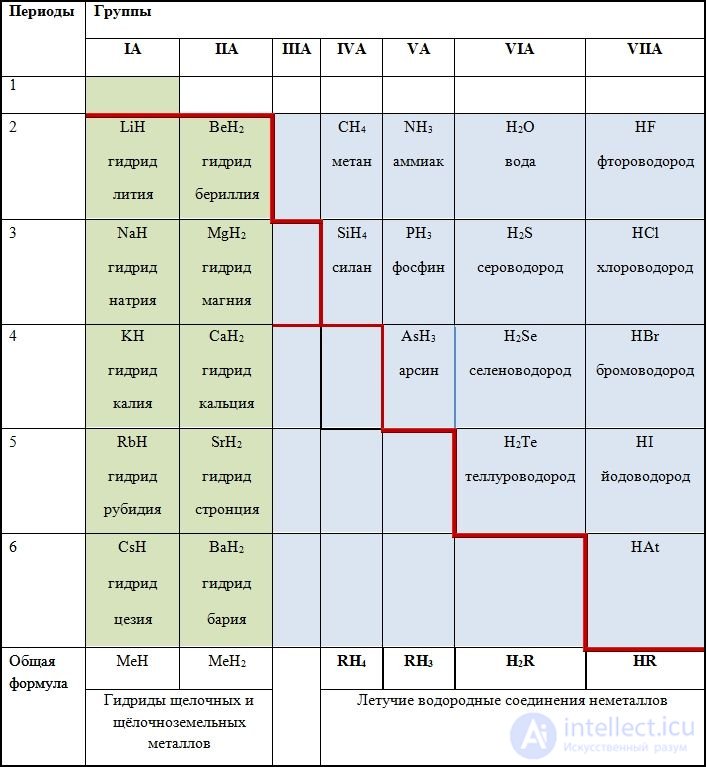
Рис. Об этом говорит сайт https://intellect.icu . 67.1. Водородные соединения некоторых металлов и неметаллов
Водородные соединения металлов IA- и IIA-групп (s-элементов, кроме бериллия) — ионные гидриды. Это белые кристаллические вещества с достаточно высокими температурами кипения, их расплавы электропроводны.
Важнейшим свойством гидридов металлов является их взаимодействие с водой и кислотами с образованием водорода:
LiH + Н2О = LiOH + H2↑;
СаН2 + 2НСl = CaCl2 + 2H2↑.
Ионные гидриды — это вещества, при нагревании разлагающиеся на металл и водород без плавления: 2NaH = 2Na + H2.
Исключение составляют LiH и CaH2, которые плавятся без разложения, но при дальнейшем нагревании все же разлагаются.
Ионные гидриды металлов обладают восстановительными свойствами:
NaH + C2H5OH = C2H5ONa + H2.
Благодаря восстановительным свойствам ионные гидриды используют для получения металлов из их оксидов или галогенидов, удаления окалины с поверхности тугоплавких металлов. Гидриды — источники водорода и поэтому перспективны как компонент ракетного топлива.
При взаимодействии ионных гидридов с гидридами алюминия или бора образуются комплексные гидриды. Из них наибольшее значение имеют борогидрид натрия Na[BH4] и алюмогидрид лития Li[AlH4] как сильные восстановители:
2RCHO + 2Li[BH4] + 2H2O = 2RCH2OH + 2LiOH + B2H6↑ (восстановление альдегидов);
2Ni2+ + + 4OH− → 2Ni +
+ 2H2↑ (восстановление ионов металлов в процессах получения металлических покрытий и порошков).
Кислотные свойства водных растворов водородных соединений неметаллов в периодах усиливаются.
Гидриды s-элементов (металлов) — ионные соединения. Они обладают восстановительными свойствами, гидролизуются и реагируют с кислотами с образованием водорода.
1. Назовите общие формулы водородных соединений элементов VIIA-, VIA-, VA- и IVA-групп.
2. Выпишите формулы водородных соединений с ковалентной связью: HCl, СаН2, Н2Se, LiH, HF, BaH2, NaH.
3. Определите степени окисления атомов в следующих гидридах:
4. Составьте уравнения синтеза гидридов, указанных в задании 3.
5. Назовите водородные соединения неметаллов, между молекулами которых существует сильная водородная связь. Объясните причину этого явления.
6. Составьте уравнения реакций между гидроксидом калия и водородными соединениями фтора и йода в молекулярной и ионной формах. Почему сумма коэффициентов в уравнениях, написанных в ионной форме, различна?
7. Составьте уравнения реакций согласно схеме:
Дайте характеристику реакциям 1* по известным вам классификационным признакам.
8. Имеется ряд водородных соединений: NaH, BaН2, Н2О, NН3, HCl. Какие из них за счет атомов водорода могут проявлять свойства:
9. Бинарное соединение кальция и неметалла VА-группы массой 1,82 г при действии воды образует газ объемом 448 см3 (н. y.). Установите химическую формулу газообразного соединения.
10. Смесь, содержащую хлор массой 35,5 г и водород массой 1,5 г, подожгли. Определите объемные доли каждого из компонентов в смеси газов после окончания реакции.
1. Летучими водородными соединениями являются вещества, формулы которых:
2. Кислотные свойства усиливаются в водных растворах соединений в ряду:
3. При растворении в воде образуют щелочь соединения:
4. Атомы водорода могут проявлять только окислительные свойства в составе:
5. В четырех пробирках находятся дистиллированная вода, а также продукты растворения в воде аммиака, бромоводорода и гидрида кальция. Результаты испытания содержимого пробирок универсальным индикатором следующие:
 |
1 – рН = 10 |
| 2 – рН = 7 | |
| 3 – рН = 13 | |
| 4 – рН = 2 |
Вода и раствор бромоводорода находятся в пробирках:
Исследование, описанное в статье про водородные соединения, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое водородные соединения и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Неорганическая химия
Из статьи мы узнали кратко, но содержательно про водородные соединенияОтветы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Неорганическая химия
Термины: Неорганическая химия