Лекция
Привет, Вы узнаете о том , что такое 38. Сложные эфиры, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое 38. Сложные эфиры , настоятельно рекомендую прочитать все из категории Органическая химия.
Изучая карбоновые кислоты, мы познакомились с реакцией этерификации — образованием сложного эфира при взаимодействии карбоновой кислоты со спиртом:
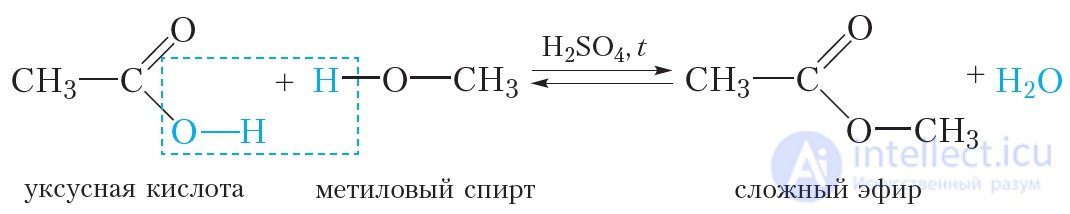
Название сложного эфира составляют из названий спирта и кислоты, из которых он образуется. Например, приведенный выше сложный эфир образовался из метилового спирта и уксусной кислоты, поэтому его название — метиловый эфир уксусной кислоты. Существует другой способ построения названий сложных эфиров. В этом случае исходят из названия соответствующего кислотного остатка (табл. 33.1) и связанного с ним радикала. В приведенном выше сложном эфире остаток уксусной кислоты (ацетат) связан с метильным радикалом. Такой сложный эфир называется метилацетатом.
Рассмотрим другой пример. Дадим название сложному эфиру:
Как видно, данный эфир образован остатками этилового спирта и муравьиной кислоты. Название данного эфира — этиловый эфир муравьиной кислоты, или этилформиат.
Сложные эфиры простейших карбоновых кислот и спиртов представляют собой жидкости, часто имеющие приятный запах фруктов или цветов.
Например, пентиловый эфир уксусной кислоты имеет запах груш, пентиловый эфир бутановой кислоты — запах абрикосов, бутиловый эфир бутановой кислоты — ананасов и т. д. Действительно, приятные запахи цветов и фруктов часто обусловлены наличием в их составе сложных эфиров.
Сложные эфиры получают по уже известной вам реакции этерификации. Например, этиловый эфир уксусной кислоты можно получить из этанола и уксусной кислоты:
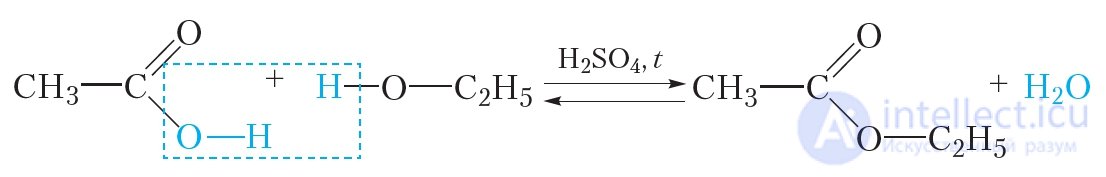
Серная кислота выступает в роли катализатора. Для проведения данной реакции используют концентрированные (практически не содержащие воду) растворы этилового спирта, уксусной и серной кислот. В результате нагревания смеси исходных веществ, сложный эфир удаляется из реакционной смеси в виде газа и затем конденсируется в пробирке-приемнике: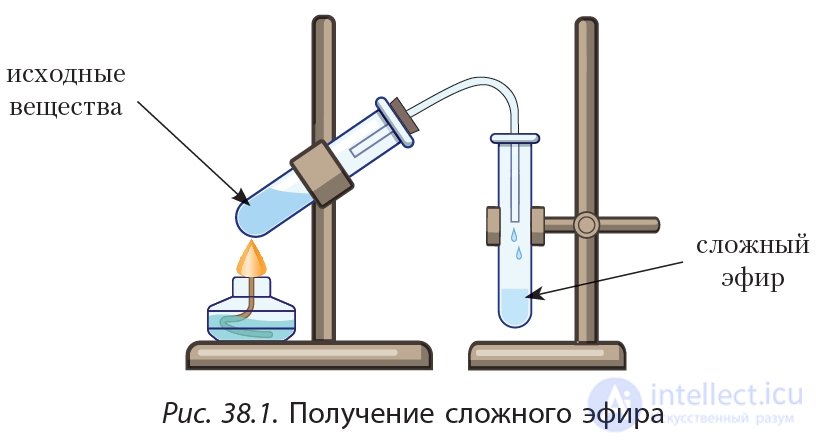
Удаление этилового эфира уксусной кислоты из реакционной смеси объясняется тем, что среди всех участвующих в реакции веществ этиловый эфир уксусной кислоты имеет наименьшую температуру кипения tкип = 77 °С. Об этом говорит сайт https://intellect.icu . Сравнительно невысокая температура кипения сложного эфира обусловлена тем, что в его молекуле отсутствуют полярные группы —OH, следовательно, между молекулами эфира не могут образовываться водородные связи. В молекулах воды, этанола, уксусной и серной кислот содержатся группы —OH, поэтому в этих веществах имеются водородные связи и их температуры кипения выше, чем у этилового эфира уксусной кислоты.
Кислотный гидролиз
Важное химическое свойство сложных эфиров — взаимодействие их с водой в присутствии серной кислоты, приводящее к образованию карбоновой кислоты и спирта. Эта реакция называется кислотным гидролизом сложного эфира: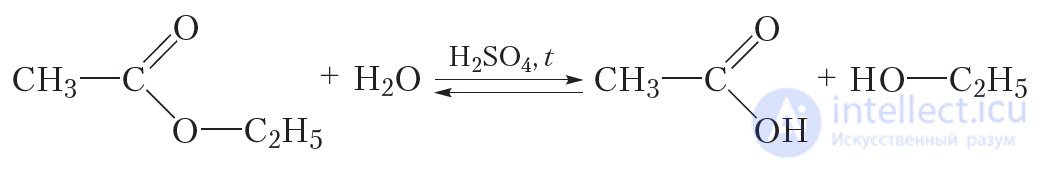
Как видно, реакция гидролиза сложного эфира является реакцей, обратной реакции этерификации. Если для проведения реакции этерификации использовались концентрированные (практически не содержащие воду) растворы исходных веществ, то гидролиз, наоборот, проводят в избытке воды.
Щелочной гидролиз
Для того чтобы предотвратить обратную реакцию — взаимодействие образующихся спирта и кислоты с образованием эфира — можно проводить гидролиз в присутствии щелочи (щелочной гидролиз). В таком случае, щелочь будет превращать карбоновую кислоту в соль и тем самым устранять возможность протекания обратной реакции:
Благодаря приятному запаху сложные эфиры применяются в производстве фруктовых вод, кондитерских изделий, косметики. Некоторые сложные эфиры, например этиловый эфир уксусной кислоты, применяют в качестве растворителей.
Синтетическое волокно лавсан является сложным эфиром полимерного строения. Его получают в результате взаимодействия терефталевой кислоты и этиленгликоля:
 Как видно, вещества взаимодействуют между собой по типу многократно повторяющейся реакции этерификации, в результате образуются макромолекулы лавсана и низкомолекулярный продукт — вода. Напомним, что процессы, в результате которых из низкомолекулярных веществ образуется высокомолекулярное соединение и побочный низкомолекулярный продукт, называются поликонденсацией (§ 30). Так как лавсан является продуктом многократно повторяющейся реакции этерификации, его можно назвать полиэфиром, поэтому лавсан относится к синтетическим полиэфирным волокнам. В нашей стране лавсан получают на ОАО «Могилевхимволокно».
Как видно, вещества взаимодействуют между собой по типу многократно повторяющейся реакции этерификации, в результате образуются макромолекулы лавсана и низкомолекулярный продукт — вода. Напомним, что процессы, в результате которых из низкомолекулярных веществ образуется высокомолекулярное соединение и побочный низкомолекулярный продукт, называются поликонденсацией (§ 30). Так как лавсан является продуктом многократно повторяющейся реакции этерификации, его можно назвать полиэфиром, поэтому лавсан относится к синтетическим полиэфирным волокнам. В нашей стране лавсан получают на ОАО «Могилевхимволокно».|
Сложные эфиры образуются при взаимодействии карбоновых кислот со спиртами — реакция этерификации. Названия сложных эфиров составляют из названий спирта и кислоты, из которых они образуются. Сложные эфиры простейших карбоновых кислот и спиртов — жидкости с приятными запахами. Сложные эфиры взаимодействуют с водой с образованием соответствующей карбоновой кислоты и спирта. Синтетическое полиэфирное волокно лавсан получают в результате реакции поликонденсации между терефталевой кислотой и этиленгликолем.
|
1. Укажите шаростержневую модель метилового эфира муравьиной кислоты:
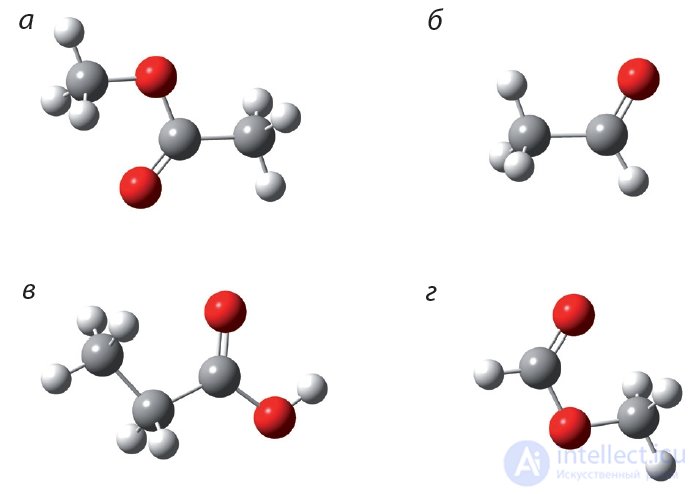
2. Напишите уравнение реакции этерификации между муравьиной кислотой и этиловым спиртом. Назовите образующийся сложный эфир.
3. Напишите структурные формулы метилового эфира муравьиной кислоты, этилового эфира муравьиной кислоты и метилового эфира уксусной кислоты. Какие из этих веществ являются изомерами?
4. Вычислите массу этилового эфира уксусной кислоты, который может быть получен при взаимодействии 30 г уксусной кислоты с 40 г этилового спирта, если выход продукта реакции составляет 75 %.
5*. Структурную формулу макромолекулы полимера, полученного в результате реакции поликонденсации, можно представить следующим образом:
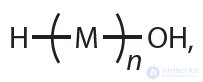
где М — структурное звено полимера, n — число остатков мономера в макромолекуле, Н— и —ОН концевые группы макромолекулы.
В результате взаимодействия этиленгликоля с терефталевой кислотой образовался полимер, в котором число остатков обоих мономеров одинаково. Определите среднее число остатков этиленгликоля в макромолекуле, если известно, что масса вступившего в реакцию этиленгликоля равна 1,86 г, а масса образовавшейся воды 1,0567 г.
6*. Как из этилена получить этилацетат? Напишите уравнения реакций.
7*. Как из карбида кальция и неорганических веществ получить этиловый эфир уксусной кислоты? Напишите уравнения реакций.
8*. В результате сжигания 740 мг органического вещества в избытке кислорода образовалось 540 мг воды и 672 см3 углекислого газа (н. у.). Известно, что данное органическое вещество представляет собой бесцветную жидкость с приятным запахом, в присутствии щелочи оно подвергается гидролизу, в результате которого образуются два органических вещества.
а) Установите структурную формулу данного органического вещества. Напишите уравнение реакции его гидролиза в присутствии щелочи. Данное органическое вещество имеет изомер, представляющий собой бесцветную жидкость с резким запахом, окрашивающую раствор лакмуса в розовый цвет.
б) Напишите структурную формулу, название этого изомера и уравнение реакции его взаимодействия с питьевой содой.
(Ответ:
а) Простейшая формула С3Н6О2.
Данной простейшей формуле отвечает этилформиат НСООС2Н5.
б) Его изомером, обладающим кислотными свойствами, является уксусная кислота.)
Исследование, описанное в статье про 38. Сложные эфиры, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое 38. Сложные эфиры и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Органическая химия
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Органическая химия
Термины: Органическая химия