Лекция
Привет, Вы узнаете о том , что такое коллоидная химия, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое коллоидная химия , настоятельно рекомендую прочитать все из категории Коллоидная химия и химия дисперсных систем.
Колло́идная хи́мия (др.-греч. κόλλα — клей) — наука о дисперсных системах и поверхностных явлениях, возникающих на границе раздела фаз. Изучает адгезию, адсорбцию, смачивание, коагуляцию, электро-поверхностные явления в дисперсных системах. Разрабатывает технологии строительных материалов, бурения горных пород, золь-гель-технологии. Играет фундаментальную роль в современной нанотехнологии, медицине, биологии, геологии, технологии производства сырья, продуктов питания и товаров различного назначения.
Современная коллоидная химия — это наука на стыке химии, физики, биологии. Особое междисциплинарное положение коллоидной химии подчеркивается тем, что в англоязычной литературе часто используют названия «коллоидная наука» (англ. colloid science) или «наука о границах раздела» (англ. interface science).
Объектом коллоидная химия являются дисперсные системы, которые находятся между истинными растворами.
и механическими смесями Дисперсии количественно оценивают дисперсностью D =1/а[м-1]. Коллоидные системы (КС) D = 107 – 109
. Истинные растворы; D>109
Механические смеси D< 107
Коллоидная химия как наука имеет непродолжительную историю, однако свойства коллоидных систем и коллоидно-химические процессы человек использовал с давних времен. Это, например, такие ремесла, как получение красок, керамики, глазури, прядение льна, хлопка, шерсти, выделывание кож.
Начиная с XVIII века появляются описания отдельных исследований, позже вошедшие в соответствующие разделы коллоидной химии. К ним относят работы М. В. Ломоносова по кристаллизации, получению цветных стекол с применением дисперсии металлов (1745—1755 гг.). В 1777 г. К. Шееле и Ф. Фонтана независимо друг от друга обнаружили явление адсорбции газов углем. В 1785 г. Т. Е. Ловиц обнаружил явление адсорбции из растворов. П. Лаплас в 1806 г. получил первые количественные отношения для капиллярного давления. В 1808 г. Ф. Ф. Рейсс, проводя опыты с элементом Вольта, открыл явления электрофорез и электроосмос.
Одни из наиболее ранних исследований коллоидных систем выполнены итальянцем Ф. Сельми в 1845 году. Он изучал системы, представляющие собой хлорид серебра, серу, берлинскую лазурь, распределенные в объеме воды. Эти системы, полученные Сельми, очень похожи на истинные растворы, однако Сельми полагал, что ни изученные им, ни другие подобные вещества не могут находиться в воде в виде таких же мелких частиц, как и образующиеся в истинных растворах, то есть в виде отдельных молекул или ионов.
Взгляды, близкие к Сельми, высказывал К. Нэгели, считавший, что в таких системах частицы серы, хлорида серебра и других веществ — более крупные агрегаты, чем отдельные молекулы. Для полимолекулярных агрегатов он ввел понятие «мицелла». Чтобы отличать системы, содержащие мицеллы, от растворов, где растворенное вещество находится в виде отдельных молекул, Нэгели назвал мицеллосодержащие системы «золями». Термины «мицелла», «золь» стали общепринятыми.
М. Фарадей в 1857 году исследовал системы, содержащие золото, распределенное в объеме воды, известные еще алхимикам, получившим их восстановлением солей золота и давшим их им название aurum potabile (питьевое золото). Изучая оптические свойства золей золота, М. Фарадей пришел к выводу, что золото в них содержится в виде очень маленьких частиц.
Основоположником коллоидной химии принято считать Т. Грэма, выполнившего в 60-х годах XIX века первые систематические исследования коллоидных систем (золей). Ему же принадлежит и введение термина «коллоид». Впоследствии коллоидная химия включила в себя результаты, полученные в других областях физики и химии, и в конце XIX — начале XX веков сформировалась в самостоятельный раздел химии.
На основе механической теории капиллярности, разработанной в начале XIX века Т. Юнгом и П. Лапласом, и термодинамики поверхностных явлений, созданной Дж. У. Гиббсом в 1878, были сформулированы основные направления исследования коллоидной химии: изучение процессов образования новой фазы в гомогенных системах, термодинамическая устойчивость коллоидных систем, количественное описание адсорбции на границе раздела фаз. Развитые в 1853 Г. Гельмгольцем представления о строении двойного электрического слоя позволили дать объяснение электрокинетическим и электрокапиллярным явлениям. Создание Дж. Рэлеем теории рассеяния света способствовало количественному изучению оптических свойств коллоидных систем. Исследование Ж. Перреном, Т. Сведбергом и Р. Зигмонди броуновского движения коллоидных частиц на основе теории, разработанной в 1905 А. Эйнштейном и М. Смолуховским, позволило доказать реальность существования молекул и правильность молекулярно-кинетических представлений. На основе предложенной в 1917 И. Ленгмюром кинетической теории адсорбции были разработаны методы исследования состояния молекул поверхностно-активных веществ (ПАВ) в мономолекулярных слоях. В 1928 П. А. Ребиндер открыл адсорбционное понижение прочности (эффект Ребиндера) и в 40—50-х годах на основе развития этого направления и исследования структурообразования в дисперсных системах создал физико-химическую механику. Физическая теория устойчивости коллоидных систем была разработана в 1937 Б. В. Дерягиным совместно с Л. Д. Ландау и независимо от них Э. Фервеем и Я. Овербеком (теория ДЛФО). Дерягиным же введено представление о механизме действия тонких слоев жидкости расклинивающее давление.
Наука о межфазных и коллоидных процессах долгое время оставалась эмпирической. Существовали отдельные математические модели, такие как электрокинетические теории Мариана Смолуховского в 1903 году или теория броуновского движения Альберта Эйнштейна в 1905 году Однако это были исключения, подчеркивающие более эмпирический подход к основной проблеме этой науки, включая стабильность коллоидов и тонких пленок.
Ситуация кардинально изменилась после изобретения теории ДЛВО в 1940-х годах школами Бориса Дерягина и Теодора Овербека . Об этом говорит сайт https://intellect.icu . Прогресс теории ДЛВО был описан Пьерандреа Ло Ностро и Барри Нинхэмом в 2019 году следующим образом:
Таким образом, всего за одно поколение коллоидная наука переместилась из захолустья физической химии, словно лужи в грязи, на передний план теоретической физики!
Дальнейшие исследования, проведенные многими различными группами, выявили трещины в основах науки о межфазных и коллоидных процессах. Две основные проблемы были сформулированы Нинханом и соавторами в нескольких статьях. Первая связана с взаимодействием между макроскопическим электростатическим двойным слоем и силами Ван дер Ваальса . Вторая связана с ролью растворенного газа и его самоорганизацией, которая игнорируется в современных теориях.
Практическое использование дисперсных материалов и связанных с ними процессов и поверхностных явлений, было известно в первоначальной ремесленной химии еще во времена глубокой древности, отстоящие от нас на тысячелетия и относящиеся к древней культуре Индии, Китая, Египта, Греции и других стран (краски и окрашивание тканей, керамика и глазури, цветное стекло, изготовление мыл и др.). Однако свою историю коллоидная химия отсчитывает с 1861 года, с открытия Т.Грэмом коллоидных растворов. Коллоидами Грэм назвал вещества, которые образуют водные растворы с клееподобными свойствами и не проходят через полупроницаемые перегородки – мембраны. По гречески колла æωλλα) означает клей, эидос (ei∆oσ) означает вид. ( В коллоидных растворах мельчайшие частицы вещества образуют одну фазу, а среда, в которой они находятся,– другую. Вещества, дающие молекулярные или ионные растворы, Грэм назвал кристаллоидами. Эти вещества, как писал Грэм в своей работе «Диффузия жидкостей в применении к анализу», не задерживаются мембраной.


Далее следовал “химический” период развития коллоидной химии, и до конца ХIХ в. усилия исследователей были направлены на синтез различных коллоидов – неорганических, органических, белковых. Уже к 1910 году было известно несколько методов получения хлорида натрия – типичного «кристаллоида» в коллоидном состоянии в органических средах. Позднее П. Веймарн получил более 200 золей из типичных кристаллоидов. Таким образом, стала понятна условность названия «коллоиды» и пришло понимание того, что большинство веществ могут быть получены в коллоидном, т.е. дисперсном состоянии, которое обеспечивает появление специфических свойств. Все это позволило говорить о коллоидном состоянии вещества как о всеобщем состоянии материи, промежуточном между молекулярным (атомы, ионы, молекулы) и фазовым (макротела). Важно понимать, что свойства вещества в коллоидном состоянии определяет не их природа, а размер частиц. Исследования зависимости свойств систем от размера частиц составили содержание следующего этапа в развитии представлений об объектах коллоидной химии. Главным результатом этого этапа явился вывод о том, что к признакам объектов коллоидной химии относится не только дисперсность, но и гетерогенность (многофазность). В начале ХХ в. в коллоидную химию вошли идеи и методы физики и физической химии. Они быстро привели к фундаментальным открытиям: установлена гетерогенная природа коллоидных растворов; открыто седиментационно-диффузионное равновесие в суспензиях и эмульсиях; разработан метод измерения размера высокодисперсных частиц и макромолекул с помощью ультрацентрифуг; создана кинетическая теория адсорбции и строения адсорбционных слоев поверхностно-активных веществ. В сочетании с термодинамикой поверхностных явлений Гиббса эти работы составили теоретический фундамент коллоидной химии.
Современная коллоидная химия – своеобразная пограничная область знания. Тесные контакты с другими науками способствовали созданию экспериментальной базы, объединяющей собственные, исторически сложившиеся, и современные методы исследования, заимствованные из других наук.
Классические коллоидно-химические методы исследования: Определение поверхностного натяжения, в частности, методом наибольшего давления пузырьков, определение поверхностного давления, ультрамикроскопия, диализ, ультрафильтрация, дисперсионный анализ, порометрия, рассеяние света и др. Методы исследования, заимствованные из других наук: Рентгенофазовый анализ, всевозможные спектральные методы (ЯМР, ЭПР, оптическая, УФ- и ИК-спектроскопии, гашение люминисценции, эллипсометрия), все виды электронной микроскопии (просвечивающая, сканирующая), атомносиловая микроскопия, флуоресцентная микроскопия и др. Перспективны современные физические методы исследования поверхности с использованием медленных электронов, масс-спектрометрия вторичных ионов и т.п.
Основные направления современной коллоидной химии:
Поскольку дисперсное состояние материи универсально и объекты изучения коллоидной химии весьма разнообразны, коллоидная химия тесно связана с физикой, биологией, геологией, почвоведением, медициной и др.
Тенденция развития коллоидной химии на современном этапе: химические процессы в коллоидных системах (химические реакции в микроэмульсиях, тонких пленках, адсорбционных слоях, пенах, гелях; мицеллярный катализ и т. п.). Современная коллоидная химия – крупная область химической науки, изучающая свойства веществ в дисперсном состоянии и поверхностные явления в дисперсных системах. Поверхностные явления (ПЯ) – процессы, происходящие на границе раздела фаз, в межфазном поверхностном слое, и возникающие в результате взаимодействия сопряженных фаз, имеющих различный состав и строение. Понятие “поверхность” в коллоидной химии отлично от геометрического.
В геометрии
Поверхность имеет площадь, но не имеет толщины. Это общая часть двух смежных областей пространства.
В коллоидной химии
Поверхность раздела фаз – это граничная область между фазами, конечный по толщине слой, в котором происходит изменение свойств от значений, характерных для одной фазы, до значений, характерных для другой.
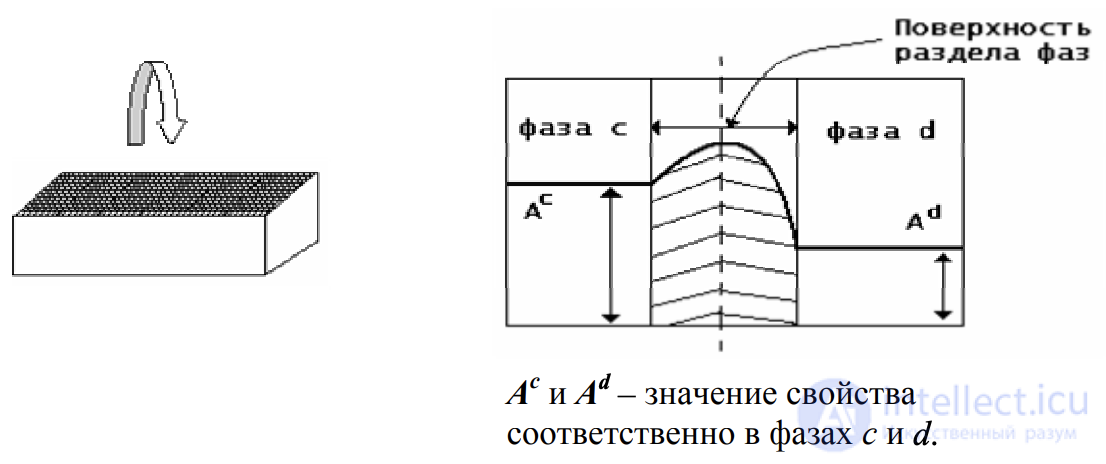
Итак, поверхность раздела фаз – это не просто граница, не имеющая толщины. На границе раздела фаз формируется поверхностный слой (межфазная поверхность) толщиной в один или несколько молекулярных размеров (диаметров). Гиббс рассматривал поверхностный слой как отдельную фазу. Теория Гиббса рассматривает поверхностный слой вещества как самостоятельную фазу, термодинамические параметры которой отличаются от аналогичных параметров объемной фазы того же вещества. Например, структура поверхности жидкости будет отличаться от структуры жидкости во внутреннем объеме. В чем же причина поверхностных явлений? Пусть из двух соседних фаз в первой межмолекулярные взаимодействия сильнее, чем во второй. Тогда в этой фазе важнейшее свойство поверхностного слоя состоит в том, что находящиеся в нем молекулы обладают избыточной энергией Гиббса (по сравнению с молекулами внутренней части той же фазы). Для внутренних молекул равнодействующая всех межмолекулярных взаимодействий равна нулю, а для поверхностных молекул она направлена перпендикулярно поверхности внутрь фазы. Догадались почему?
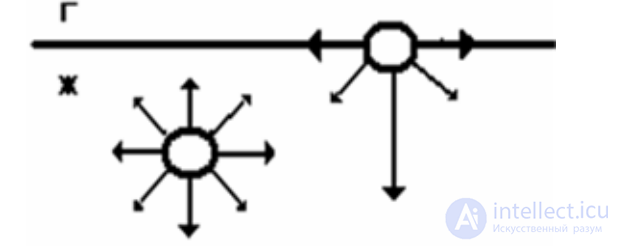
Следовательно, для выведения молекул из объема на поверхность надо преодолеть эту силу, т. е. совершить работу и сообщить молекулам определенную энергию. Увеличение площади поверхности приводит к увеличению числа поверхностных молекул и поверхностная энергия возрастает. Следовательно, молекулы, находящиеся в поверхностном слое, являются «особыми» с точки зрения энергетического состояния. Доля особых молекул возрастает с уменьшением размера частиц. Поверхностные явления присущи всем системам, имеющим поверхность раздела фаз, но сильнее всего они проявляются в дисперсных системах, которые являются гетерогенными и имеют высокоразвитую поверхность.
Схематическое изображение дисперсной системы 1-дисперсионная среда ДС (сплошная фаза) 2-дисперсная фаза ДФ (раздробленная фаза) Дисперсные системы – такие многофазные системы (например, двухфазные), где по крайней мере одна из фаз является раздробленной (т. е. представлена более или менее крупными частицами) и распределена во второй (непрерывной) фазе. Необходимым условием существования дисперсных систем является нерастворимость ДФ в ДС.
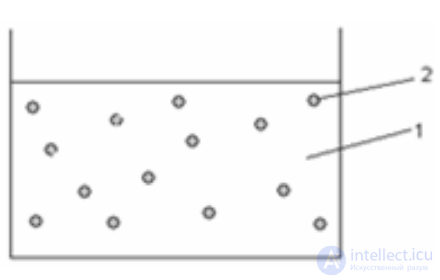
Дисперсные системы – такие многофазные системы (например, двухфазные), где по крайней мере одна из фаз является раздробленной (т. е. представлена более или менее крупными частицами) и распределена во второй (непрерывной) фазе. Необходимым условием существования дисперсных систем является нерастворимость ДФ в ДС. 7 Реальный окружающий нас мир, как и мы сами, состоит из дисперсных систем:


3. КС получают либо конденсацией, либо диспергированием.
Конденсационные методы: физические (выпаривание – конденсация) и химические
(получение нерастворимых веществ в реакциях обмена или замены растворителя).
Диспергационные методы: механические и ультразвуковые реализуют в присутствии
ПАВ (поверхностно-активных веществ).

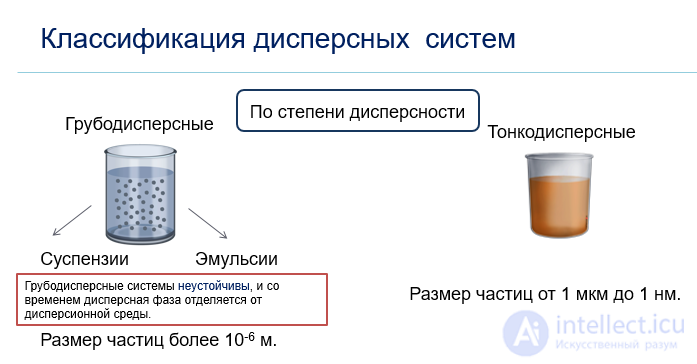
Составными частями КС являются дисперсная фаза (ДФ) и дисперсионная Среда (ДС). Коллоидные растворы имеют название – золь.
По взаимодействию между собой частиц ДФ различают бесструктурные и структурированы Коллоидные системы. По взаимодействию между собой ДФ и ДС различают лиофобные и лиофильные Коллоидные системы.
Классифицируют Коллоидные системы по агрегатному состоянию ДФ и ДС.
| Дисперсная фаза (ДФ) | Дисперсионная среда (ДС) | Тип системы | Пример |
|---|---|---|---|
| Газ | Жидкость | Газ в жидкости | Пена |
| Газ | Твердое | Газ в твердом | Пемза |
| Жидкость | Газ | Жидкость в газе | Туман |
| Жидкость | Жидкость | Жидкость в жидкости | Эмульсия |
| Жидкость | Твердое | Жидкость в твердом | Грунт |
| Твердое | Газ | Твердое в газе | Дым |
| Твердое | Жидкость | Твердое в жидкости | Суспензия |
| Твердое | Твердое | Твердое в твердом |
Сплав |
Частицы какого размера следует рассматривать как коллоидные? Коллоидные частицы занимают промежуточное положение между атомами и реальными объектами:
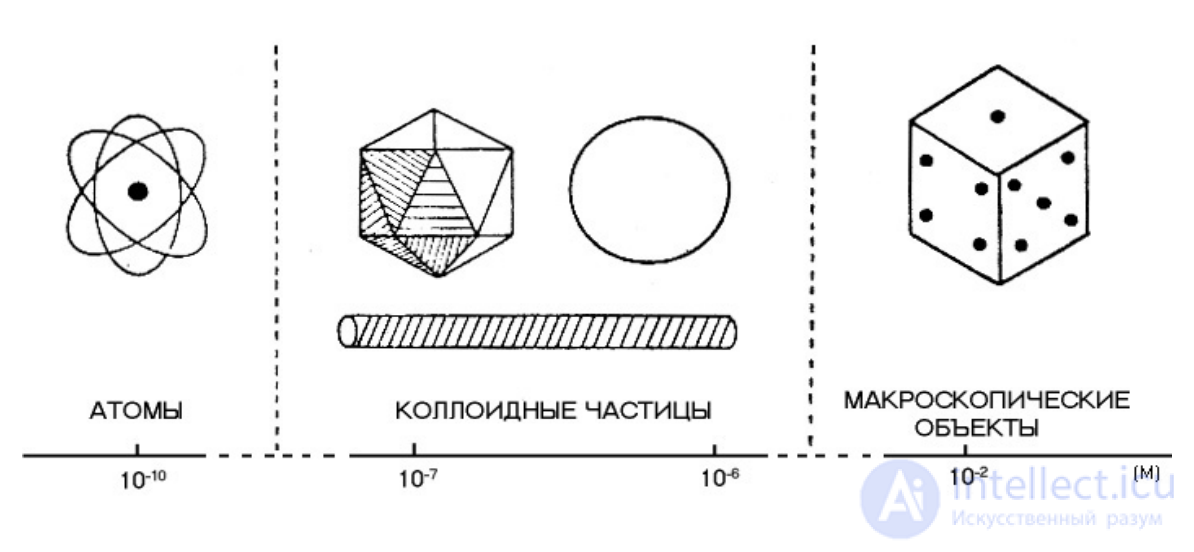
Если представить себе обычную молекулу величиной с маленькую крупинку сахара, то коллоидные частицы средних размеров оказались бы величиной с яблоко! Термин “коллоид” относится к любому веществу независимо от его химического состава, структуры, геометрической формы, агрегатного состояния, если по крайней мере один из его размеров менее 1 мкм, но более 1 нм. M.G.Hill. Enciclopedia of Science and Technology. 1987, Vol. 4, P. 162. Это определение дано в традиционном понимании «коллоиднодисперсных» систем, для которых характерно активное участие частиц в броуновском движении с вытекающими отсюда молекулярнокинетическими явлениями (диффузия, осмос). Рассматриваемый современной коллоидной химией диапазон размеров шире: от больших, чем простые молекулы, до видимых невооруженным глазом, т. е. от 10-9 до 10-4 м.

Форма частиц дисперсной фазы может быть различной: Электронные микрофотографии коллоидных частиц сульфидов цинка ZnS (а) и свинца PbS (b), фосфата магния Mg3(PO4)2 (с), карбоната кадмия CdCO3 (d), вируса табачной мозаики (е) и сажи (f).
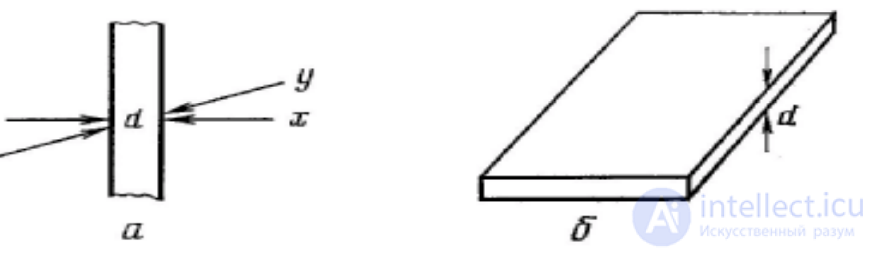
Помимо частиц в качестве дисперсной фазы могут быть нити, волокна, а также пленки. Нити (а), например, имеют два размера, определяющих дисперсность, пленки (б) – один
Если размер, определяющий дисперсность, у всех частиц одинаков, то подобную систему называют монодисперсной, например, пыльца некоторых растений, полученные синтетическим путем полимерные микросферы и т. п.
Если в системе присутствуют частицы различных размеров, то такая система называется полидисперсной.
1) Чем интересны монодисперсные коллоидные системы?
2) Что такое коллоидные кристаллы?
Исследование, описанное в статье про коллоидная химия, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое коллоидная химия и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Коллоидная химия и химия дисперсных систем
Ответы на вопросы для самопроверки пишите в комментариях, мы проверим, или же задавайте свой вопрос по данной теме.
Комментарии
Оставить комментарий
Коллоидная химия и химия дисперсных систем
Термины: Коллоидная химия и химия дисперсных систем