Лекция
Привет, Вы узнаете о том , что такое получение коллоидной системы, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое получение коллоидной системы , настоятельно рекомендую прочитать все из категории Коллоидная химия и химия дисперсных систем.
Для того, чтобы получить коллоидный раствор или золь, необходимо
выполнить два условия: 1) создать в жидкости твердые или жидкие нерастворимые частицы коллоидной степени дисперсности; 2) обеспечить устойчивость этих частиц, предохранив их от слипания друг с другом (от коагуляции), т. е. стабилизировать систему. Стабилизация коллоидных систем
может производиться путем введения в систему нового компонента – стабилизатора, который адсорбируется на поверхности коллоидных частиц и
придает частицам заряд и/или образует защитную оболочку.
Свободнодисперсные системы (порошки, суспензии, эмульсии,
золи) можно получить двумя способами: диспергированием и конденсацией.
Диспергирование основано на получении из сплошного и крупного
по размерам тела 3 более мелких частиц дисперсной фазы 2.
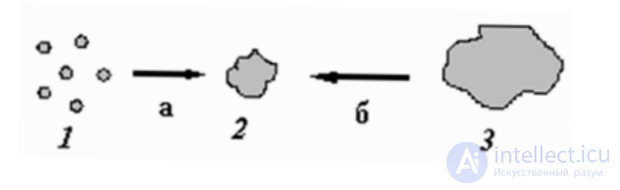
Конденсация, напротив, связана с укрупнением частиц 1, в том числе
и частиц молекулярных размеров, до частиц определенного класса дисперсных систем 2.
Мы даже не подозреваем, что во многих процессах происходит возникновение и
разрушение дисперсных систем.
Известно, что обезболивающий эффект таких препаратов, как хлороформ, диэтиловый эфир, циклопропан, связан с образованием в кровеносных сосудах головного мозга частиц дисперсной фазы из гидратных
микрокристаллов (клатратов). Продолжительность анестезии определяется временем существования клатратов. С течением времени дисперсная система разрушается и анестезирующий эффект прекращается.
Диспергирование может быть самопроизвольным и несамопроизвольным.
Самопроизвольное диспергирование характерно для лиофильных систем.
Термодинамическая возможность самопроизвольного процесса, в том
числе и диспергирования, определяется условием ∆G = ∆H – T∆S < 0.
Для диспергирования необходимо затратить определенную работу или
эквивалентное ей количество тепла. Эти затраты определяются изменением
энтальпии ∆H. Для разрушения существующих связей внутри тела необходимо преодолеть когезию (связь между молекулами, атомами или ионами)
внутри тела в пределах одной фазы и затратить определенную работу, которая называется работой когезии, Wк. Применительно к идеальному твердому телу величину Wк называют когезионной прочностью. После образования новых поверхностей раздела фаз на межфазной границе возникает
адгезия (связь между разнородными конденсированными телами при их
молекулярном контакте). В результате адгезии поверхностная энергия
уменьшается на величину, которая характеризует работу адгезии Wа. Поэтому изменение энтальпии при диспергировании можно представить в виде ∆диспH = Wк – Wа.
Поясним это условие примером. Для того, чтобы из куска теста получить несколько комков, необходимо преодолеть взаимодействие
частиц самого теста, т. е. его когезию (Wк). Вновь образовавшаяся
поверхность комков характеризуется определенной адгезией по отношению к окружающей среде, т. е. адгезией между тестом и воздухом или какой-либо другой поверхностью (Wа).
При самопроизвольном диспергировании:
∆H < 0, ∆S > 0, ∆G < 0, Wа > Wк
К лиофильным системам относятся критические эмульсии, высокодисперсные золи парафина в углеводородах, водные растворы эмульсолов – углеводородов с большим содержанием (10-40 %) мыл и растворы мицеллообразующих ПАВ и т. д.
Согласно Ребиндеру и Щукину самопроизвольное отщепление частиц
коллоидных размеров от макрофазы возможно, если межфазное натяжение
мало. В этом случае работа, затрачиваемая на образование новой поверхности, компенсируется уменьшением энтальпии в процессе сольватации и
ростом энтропии за счет участия образующихся частиц в броуновском движении.
Критерий Ребиндера-Щукина образования лиофильных систем:

где
d – линейный размер частиц,
β – коэффициент, учитывающий форму частиц и изменение энтропии.
При несамопроизвольном диспергировании:
∆H > 0, ∆S > 0, ∆G > 0, Wа < Wк.
Несамопроизвольное диспергирование характерно для лиофобных систем.
Здесь процесс диспергирования осуществляется за счет внешней энергии.
Примерно 5 % производимой в мире энергии расходуется на процесс
диспергирования.
Несамопроизвольное диспергирование бывает:
- механическое
- физическое (диспергирование ультразвуком, электрическими методами)
- физико-химическое (пептизация).
Механическое диспергирование в зависимости от агрегатного
состояния дисперсной фазы:
- измельчение, истирание, раздавливание и т. Об этом говорит сайт https://intellect.icu . д.;
- распыление;
- барботаж.
Измельчение проводят в мельницах различной конструкции, например
в шаровых (а) или коллоидных (б) мельницах.
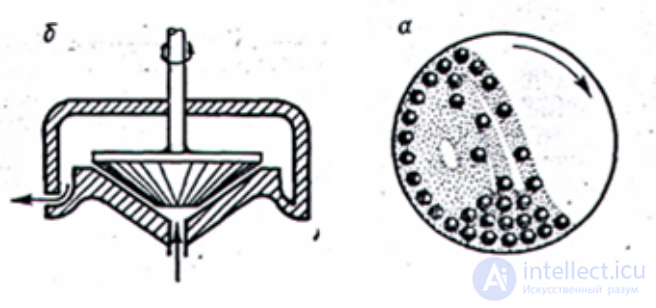
В шаровых мельницах получают частицы размером 6·104 нм при сухом помоле и менее 103 нм при мокром; в
коллоидных – 100 нм и менее.
Помол в коллоидных мельницах осуществляется очень быстро. До изобретения коллоидной мельницы графит, например, растирали на шаровых мельницах, и на это уходило 15-20 суток. Коллоидные мельницы
выполняют эту работу за 15-20 минут.
Измельчением получают системы типа Т/Г, Т/Ж, распылением – Ж/Г,
Ж/Ж, барботажем – Г/Ж.
Разрушение материалов в процессе диспергирования может быть облегчено при использовании эффекта Ребиндера – адсорбционного понижения
прочности твердых тел. Этот эффект заключается в уменьшении поверхностной энергии с помощью поверхностно-активных веществ.
Диспергирование ультразвуком высокой частоты эффективно лишь в
том случае, если диспергируемое вещество обладает малой прочностью.
При действии на суспензию ультразвука возникают механические колебания (порядка нескольких тысяч в 1 с), которые разрывают частицы на более мелкие. Таким путем получают органозоли хрупких металлов, гидрозоли серы, графита, гидроксидов металлов, различных полимеров и т. п.
При диспергировании в электрических аппаратах избыток электрических зарядов сообщается распыляемой жидкости, и в результате отталкивания одноименных зарядов происходит дробление жидкости на капли.
К физико-химическому диспергированию относится метод пептизации.
Пептизацией называют переход осадков под действием пептизаторов в состояние коллоидного раствора. Пептизировать можно только “свежие”
(свежеприготовленные) осадки, в которых частицы коллоидного размера
соединены в более крупные агрегаты через прослойки ДС. По мере хранения осадков происходят явления рекристаллизации и старения, приводящие к сращиванию частиц друг с другом, что препятствует пептизации.
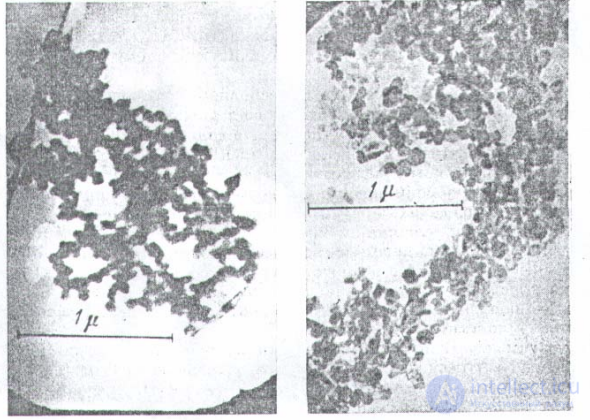
Слева - аморфные сферические частицы свежего золя гидроокиси алюминия
Справа - кристаллические частицы золя того же вещества по истечении 2-3 месяцев после приготовления золя
Различают пептизацию:
- адсорбционную;
- диссолюционную;
- промывание осадка растворителем
Рассмотрим получение золей методом пептизации на примерах:
Получение золя бромида серебра адсорбционной пептизацией.
Приготовим осадок бромида серебра AgBr:
AgNO3 + KBr → AgBr↓ + KNO3
свежий осадок
Возьмем избыток AgNO3 (который играет роль пептизатора)
ОБРАЗУЕТСЯ ЗОЛЬ, структурная единица дисперсной фазы которого называется мицеллой. Как происходит образование мицеллы??? Ионы Ag+
(потенциалопределяющие ионы) адсорбируются на поверхности частиц
осадка AgBr, заряжая их положительно, к положительно заряженной поверхности образовавшегося ядра мицеллы притягиваются ионы противоположного знака – противоионы (ионы NO3
-
). Часть этих ионов, составляющая адсорбционный слой, прочно удерживается у поверхности ядра за
счет электростатических и адсорбционных сил. Ядро вместе с адсорбционным слоем составляет коллоидную частицу. Остальные противоионы связаны с ядром только электростатическими силами. Эти противоионы образуют диффузный слой. Наличие заряда у коллоидных частиц приводит к их
отталкиванию и обеспечивает устойчивость золя.

V Получается, что мицелла в целом электрически нейтральна???
Мицеллу золя AgBr можно представить и в другом (графическом) виде:
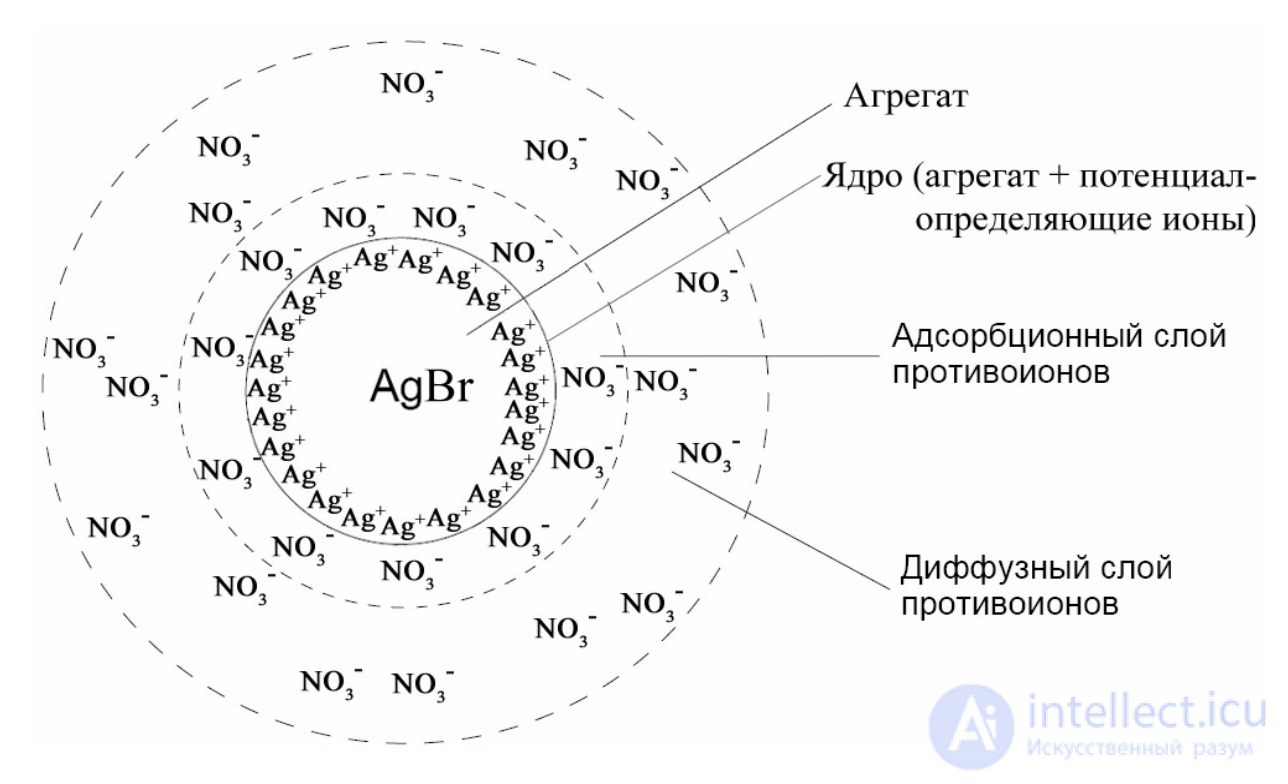
Как следует из рисунка и приведенной выше структурной формулы мицеллы, на поверхности твердых частиц осадка располагаются противопо22
ложные по знаку заряда ионы, которые пространственно разделены. Эти
ионы образуют двойной электрический слой.
Диссолюционная пептизация отличается от адсорбционной только отсутствием в готовом виде электролита-пептизатора. Рассмотрим на примере
получения золя гидроксида железа.
FeCl3 + NH4OH → Fe(OH)3↓ + NH4Cl – получили свежий осадок, который
помещаем на фильтр и осторожно добавляем HCl:
Fe(OH)3 + HCl → FeOCl + 2H2O
Образовавшийся FeOCl является электролитом – пептизатором. Далее
происходят такие же процессы, как и при адсорбционной пептизации с образованием мицелл:
{[mFe(OH)3]·nFeO+
·(n-x)Cl-
}
x+·xCl-
.
Метод промывания осадка растворителем используется, если осадок получен при значительном избытке одного из реагентов. Большая концентрация ионов в растворе вызывает сжатие двойного электрического слоя. Ионы диффузного слоя проникают в адсорбционный, в результате заряд коллоидной частицы становится равным 0 и происходит агрегация частиц:
{[mFe(OH)3]·nFe3+·3nCl-
}
0
.
После промывания осадка растворителем мицеллы будут иметь вид:
{[mFe(OH)3]·nFe3+·3(n-x)Cl-
}
3x+·3xCl-
.
Позвольте, но пептизируемый осадок – это уже диспергированный материал, доведенный до коллоидной степени измельчения, в котором
частицы в результате слипания образовали крупные агрегаты! Можно
ли метод пептизации однозначно рассматривать как диспергационный?
Ведь исходный осадок получен конденсационным методом!
Несмотря на широкое применение диспергационных методов, они (за
исключением пептизации) не могут быть использованы для получения дисперсных систем максимальной дисперсности. Такие системы получают
конденсационными методами, не требующими затраты внешней работы.
К конденсационным методам относятся конденсация, десублимация и кристаллизация.
Конденсация бывает гомогенная и гетерогенная.
Гомогенная конденсация предполагает формирование новой фазы на зародышах, самопроизвольно возникающих в результате флуктуаций плотности и концентрации в системе, а гетерогенная – формирование новой фазы
на уже имеющихся поверхностях (ядрах конденсации – стенки сосудов, частицы примесей).
Необходимое условие конденсации – пересыщение и неравновесное распределение вещества в объеме, а также образование центров конденсации или зародышей.
Различают конденсацию
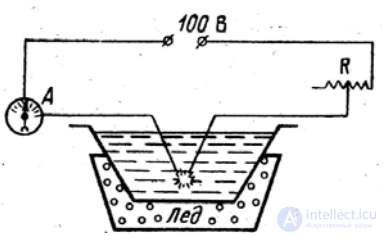
К физической конденсации относятся метод Бредига
и метод Рогинского и Шальникова. Метод Бредига
можно рассматривать как конденсационный, так и
диспергационный. Два электрода из металла
погружают в жидкость (она станет дисперсионной
средой золя), концы их сближают и пропускают
электрический ток. Возникающая дуга отчасти распыляет металл до коллоидных частиц, отчасти испаряет его, и пар конденсируется в холодной
жидкости также в виде коллоидных частиц. Таким способом получают золи
многих металлов.
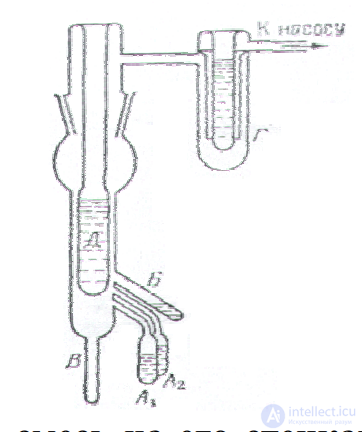
Метод Рогинского и Шальникова был предложен в 1943 году. В сосуды А1 и
А2 помещают растворитель, а в сосуд Б – вещество, которое должно быть диспергировано. Сосуды А1 и А2 погружают в жидкий воздух и весь прибор эвакуируют,
поместив на пути к насосу ловушку с жидким воздухом
Г. После этого в сосуд Д наливают жидкий воздух, и
сосуды А1, А2 и Б каждый в отдельности подогревают
электрическими нагревателями. При этом оба вещества конденсируются на сосуде Д в соотношении, которое
определяется соотношением температур в А1, А2 и Б.
Удаляют жидкий воздух из сосуда Д, причем твердая
смесь на его стенках отстаивает и в виде коллоидной дисперсии стекает в
сосуд В. Этот метод позволяет получать в очень чистом виде коллоидные
дисперсии разнообразных веществ: например, красно-фиолетовые золи натрия, сине-зеленые золи цезия в эфире, бензоле и других органических жидкостях.
К физико-химической конденсации относится метод замены растворителя, который сводится к тому, что вещество, из которого предполагается
получить золь, растворяют в соответствующем растворителе в присутствии
стабилизатора (или без него) и затем раствор смешивают с избытком другой
жидкости, в которой вещество нерастворимо. В результате образуется золь.
Так получают золи серы, канифоли.
V За счет чего в данном случае возникает пересыщение?
Химический метод конденсации основан на реакциях, приводящих к
возникновению твердого продукта. Это реакции
а) восстановления. Например, получение золей золота и серебра при
взаимодействии солей этих металлов с восстановителями:
2KAuO2 + 3HCHO + K2CO3 → 2Au + 3HCOOK + KHCO3 + H2O.
{[mAu]·nAuO2
-
·(n-x)К+
}
x-·xК+
– мицелла золя золота.
б) окисления. Например, получение золя серы:
Н2S + 1 2O2 → S + H2O.
Параллельно протекают более сложные процессы, приводящие к образованию пентатионовой кислоты H2S5O6, являющейся стабилизаторами золей
серы. Строение мицеллы полученного золя можно представить следующей
формулой:
{[mS]·nS5O6
2-·2(n-x)H+
}·2xH+
.
в) гидролиза. Например, красно-бурый золь гидроксида железа получается, если в кипящую воду добавить небольшое количество хлорида железа:
FeCl3 + H2O → Fe(OH)3 + 3HCl
Fe3+
Потенциалопределяющие ионы – FeO+
H+
Таким образом, мицелла золя Fe(OH)3 в соответствии с тем, какой ион является стабилизатором, может быть выражена формулами:
{[mFe(OH)3]·nFeO+
·(n-x)Cl-
}
x+·xClили {[mFe(OH)3]·nFe3+·3(n-x)Cl-
}
3x+·3xClили [mFe(OH)3]·nH+
·(n-x)Cl-
}
x+·xCl-
.
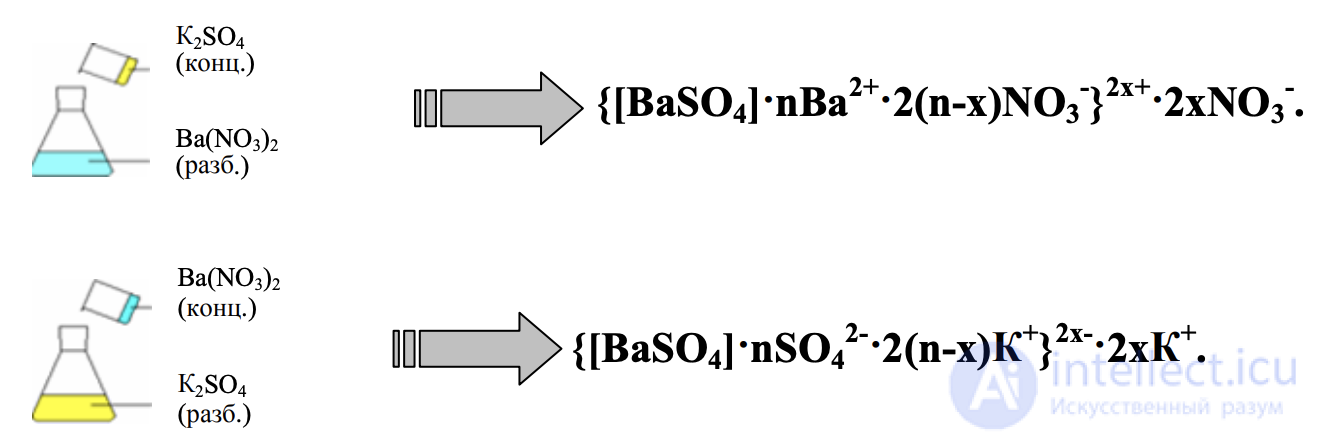
г) обмена. Например, получение золя сульфата бария.
При использовании реакций обмена состав мицелл зависит от того, в каком
порядке сливать растворы реагентов!
Примером получения коллоидных систем кристаллизацией является
кристаллизация из пересыщенного раствора сахарозы в производстве сахара. Процесс десублимации имеет место при образовании облаков, когда в
условиях переохлажденного состояния из водяных паров образуются сразу
кристаллики, а не капли воды.
Исследование, описанное в статье про получение коллоидной системы, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое получение коллоидной системы и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Коллоидная химия и химия дисперсных систем
Комментарии
Оставить комментарий
Коллоидная химия и химия дисперсных систем
Термины: Коллоидная химия и химия дисперсных систем