Лекция
Привет, Вы узнаете о том , что такое 7: ЛИОФИЛЬНЫЕ коллоидные системы, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое 7: ЛИОФИЛЬНЫЕ коллоидные системы , настоятельно рекомендую прочитать все из категории Коллоидная химия и химия дисперсных систем.
1. Особливістю цього типу КС є те, що вони термодинамічно стійкі, так як при
їх утворенні ∆G < 0.
2. Ліофільними КС є міцелярні розчини колоїдних ПАР і розчини ВМС.
3. Відмінністю розчинів ВМС від класичних КС полягає в асиметричності і
гнучкості молекул полімерів, яка обумовлює існування множинності
конформацій.
4. Критерій ліофільності КС (критерій Ребіндера – Щукіна)
α
2Ϭ ≤ βkT
Тут : α - лінійний розмір частинки, β - коефіцієнт форми частинки.
Розчини ВМС
5. Розчинення ВМС проходить через стадію набухання – поглинання
розчинника фазою ВМС. Якщо енергія сольватації невелика – набухання
обмежене. Якщо велика – то необмежене.
6. Серед ВМС особливе місце займають поліелектроліти – це полімери, до
складу яких входять іоногенні групи. Якщо одночасно присутні і кислотні (-
СООН) і основні (-NH2), то це амфоліти.
7. В залежності від умов можлива різна ступінь дисоціації груп у амфолітів,
що формує різний за знаком і величиною заряд. Це впливає на вид конформацій
ВМС і на стабільність розчину. Об этом говорит сайт https://intellect.icu . Молекулярна форма ВМС, коли q- = q+, існує в
ізоелектричній точці. Вона відповідає конкретному значенню pH. У цій точці
амфоліти згортаються у клубок (глобули).
Розчини ПАР
8. Дифільні ПАР здатні утворювати міцели за рахунок об’єднання в ядро їх
гідрофобних частин і створення оболонки з гідрофільних груп.
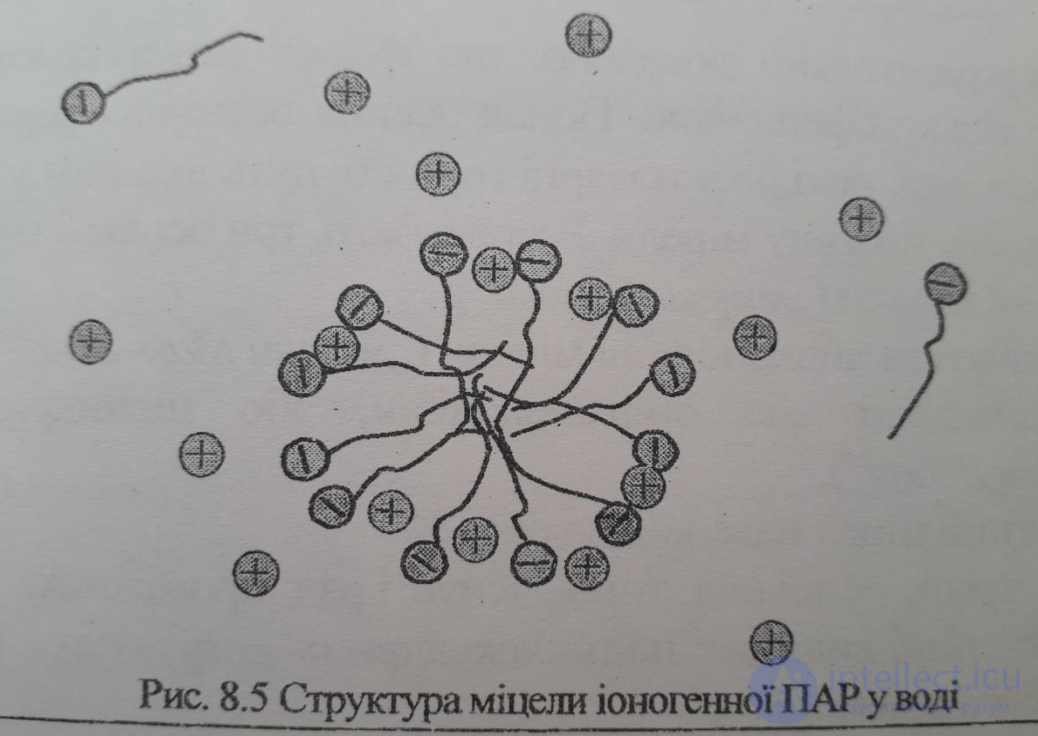
9. Здатність ПАР до міцелоутворення оцінюють по величині гідрофільно –
ліпофільного балансу (ГЛБ): це співвідношення енергій сольватації полярних і
неполярних частин ПАР.
10. ПАР з високим ГЛБ не лише здатні утворювати міцели, вони є
стабілізаторами емульсій типу масло/вода. З низьким ГЛБ – є стабілізаторами
емульсій вода/масло.
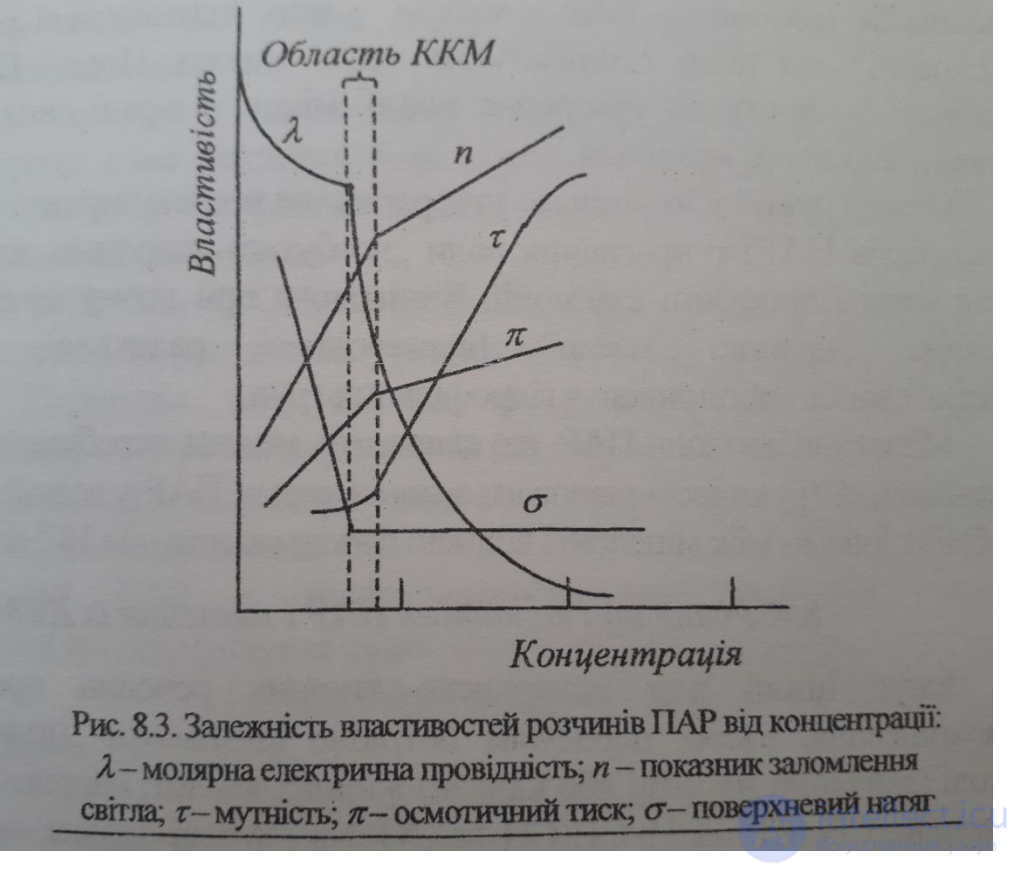
11. Міцели у розчинах колоїдних ПАР утворюються лише при досягненні
певної граничної концентрації, яку позначають абревіатурою ККМ (критична
концентрація міцелоутворення).
12. ККМ визначають в точці різкої зміни залежності «фізична властивість
розчину» - «концентрація ПАР»
13. Кількість молекул ПАР, зв’язаних у міцелу, називають числом агрегації
(Nагр.). В залежності від природи ПАР Nагр. змінюється від десятків до тисяч
одиниць.
14. Виділяють три типи міцел ПАР:
сферичні (міцели Хартлі)
пластинчаті (міцели Мак-Бена)
стержневі (міцели Дебая)
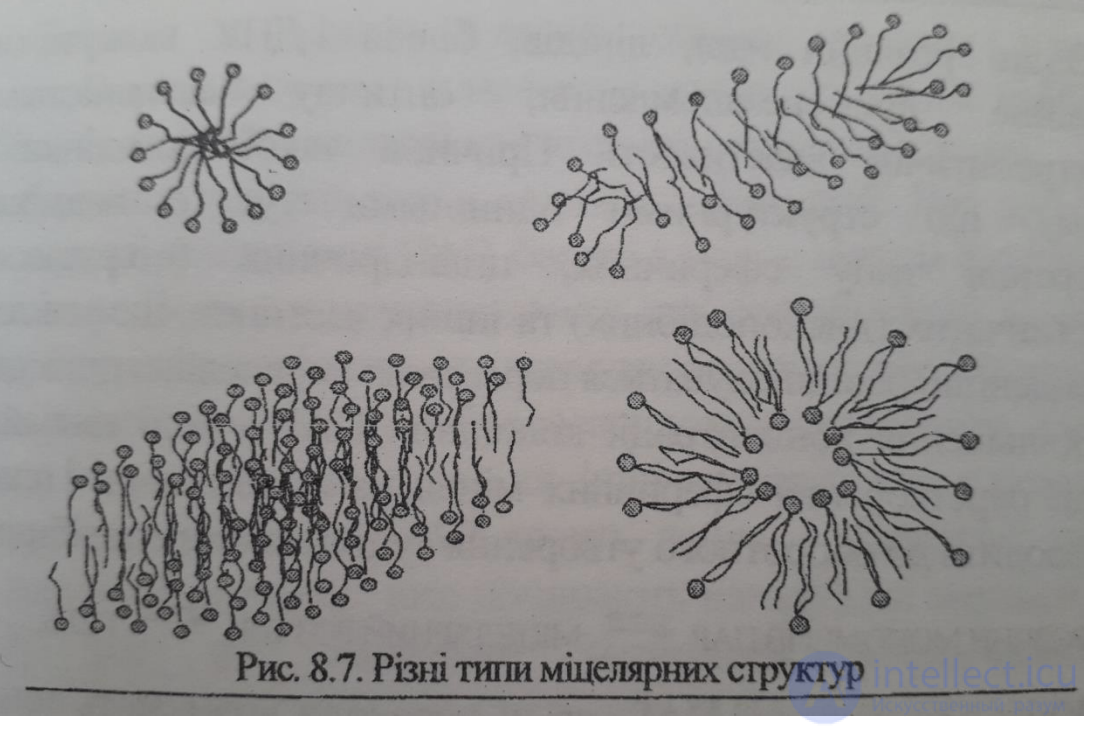
15. В залежності від умов форми міцел можуть оборотно змінюватись
(переходити одна в другу). Такі розчини мають декілька ККМ.

16. Міцелярні розчини ПАР здатні поглинати нерозчинні в ДС речовини. Це
називається солюбілізацією. Вказане явище використовується в живих організмах
(засвоєння жирів, вітамінів), фармації (подача ліків у зручних для організма
формах), хімічній технології (міцелярний каталіз, емульсійна полімеризація), в
побуті (миючі засоби).
17. Основні чинники, які обумовлюють миючу дію ПАР
Забезпечення хорошого змочування поверхні тканини, її гідрофілізація за
рахунок адсорбціі.
Дифільність ПАР забезпечує їх адсорбцію і на поверхні нерозчинних у воді
частинок бруду, що приводить до їх відділення від тканини.
Іоногенні ПАР стабілізують піну і тим самим сприяють флотації на
бульбашках повітря частинок бруду.
Міцелоутворення і солюбілізація завершають видалення дрібних частинок
бруду
Исследование, описанное в статье про 7: ЛИОФИЛЬНЫЕ коллоидные системы, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое 7: ЛИОФИЛЬНЫЕ коллоидные системы и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Коллоидная химия и химия дисперсных систем
Комментарии
Оставить комментарий
Коллоидная химия и химия дисперсных систем
Термины: Коллоидная химия и химия дисперсных систем