Лекция
Привет, Вы узнаете о том , что такое 6 : Устойчивость и коагуляция коллоидных систем, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое 6 : Устойчивость и коагуляция коллоидных систем , настоятельно рекомендую прочитать все из категории Коллоидная химия и химия дисперсных систем.
Ліофобні КС
1. ∆G цих систем >0 , тобто – вони термодинамічно нестійкі, що
проявляється у зміні концентрації часток ДФ.
2. Є два шляхи зменшення ∆G : адсорбція ПАР і об’єднання малих частинок
у великі. У першому випадку зменшується поверхнева енергія, у другому –
зменшується питома площа ДФ.
3. Розрізняють кінетичну та агрегативну стійкість КС.
Кінетична – визначається дифузійно – седиментаційним балансом
Агрегативна – визначається здатністю до злипання частинок ДФ, тобто –
природою адсорбційного шару на межі фаз ДФ і ДС.
4. Для безструктурних полідисперсних КС характерною є залежність
розчинності ДФ (L) від розміру часток (α):
ln (L1/L2) = (4 Ϭ Mr/ρRT) / (1/α1 – 1/α2)
(рівняння Гіббса – Оствальда – Фрейндліха)
5. Таким чином, в КС великі частинки зростають далі або за рахунок
поглинання малих цілком, або унаслідок поступового осадження на свою
поверхню речовини ДФ, яка є продуктом розчинення малих часток.
Перший варіант здебільшого реалізується в КС з рідкою, або газоподібною
фазою ДФ, другий – з твердою.
6. Коагуляція – об’єднання частинок ДФ (злипання).
7. Коагуляцію можна визвати, або прискорити дією різноманітних факторів:
нагрів, охолодження, опромінення, механічна дія, ультразвук, електричне поле,
хімічні реагенти, тощо.
Мінімальна інтенсивність фактору, що визиває коагуляцію, є порогом
коагуляції.
Якщо бар’єр на межі фаз має електростатичну природу – то коагуляцію можна
визвати дією сильного електроліту. Тоді поріг коагуляції (Υ) виражають у
мілімолях цього електроліту в 1л КС.
8. Об этом говорит сайт https://intellect.icu . Коагулююча дія (сила) фактору, що визвав коагуляцію,є величиною,
оберненою доΥ.
9. Поріг коагуляції визначають оптично по появі інтенсивного світлорозсіяння
в КС, внаслідок різкого збільшення розміру частинок ДФ.
10. Коагулююча дія фактору проявляється через певний час – індукційний
період, коли dʋ/dt →0. Далі йде фаза повільної коагуляції, коли зіткнень частинок
ДФ багато, але не всі завершуються об’єднанням.
11. Коли інтенсивність коагулюючого фактору досягає порогу коагуляції,
швидкість стає максимальною за рахунок того, що тут всі зіткнення завершується
об’єднанням частинок. Кінетика швидкої коагуляції описується рівнянням
Смолуховського
ʋt = ʋ0/ (1+t/Ɵ), тут Ɵ – період коагуляції, відповідає часу, коли ʋt = ʋ0/2, ʋ -
концентрація частинок ДФ.
12. Коагулюючу силу мають ті йони електроліту, що вводять у КС, які
протилежно заряджені до гранул, або іншими словами мають потенціал,
протилежний ξ- потенціалу.
13. Правило Гарді – Шульце: коагулюючи дія йона пропорційна його заряду в
ступені «n». Величина «n» залежить від радіусу йона і його гідратації.
14. Є концентраційний і нейтралізаційний механізми дії електроліту на КС.
Нейтралізаційний – адсорбція протийонів зменшує ξ.
Концентраційний – збільшення йонної сили (I) зменшує ξ.
15. Основною теорією, яка описує процес коагуляції в ліофобних КС, є теорія
Дерягіна – Ландау – Фервея – Овербека (ДЛФО).
В ній враховується, що в зоні контакту двох частинок ДФ діють слідуючі сили:
електростатична, молекулярна, адсорбційна, розклинювальний тиск
Розклинювальний тиск – створюється рівнодіючою поверхневих сил,
залежить від Ϭ.
Електростатична складова – відповідає дії електростатичного поля гранул.
Молекулярна складова – ван-дер-ваальсова взаємодія.
Адсорбційна складова – збільшення концентрації на поверхні збільшує
осмотичний тиск.
16. У спрощеному варіанті ДЛФО присутні лише електростатична і
молекулярна компоненти u = uел. + uмол. = 64CRTƛ
. ɣ
2 . exρ(-h/ƛ) – A/12πh2
Тут h – відстань між міцелами,
A – константа Гамакера,
ɣ - функція електричного потенціалу адсорбційного шару (ψa)
ƛ – товщина ПЕШ
ɣ = [exρ(ZF ψa / 2RT) – 1] / [exρ (ZF ψa / 2RT) + 1]
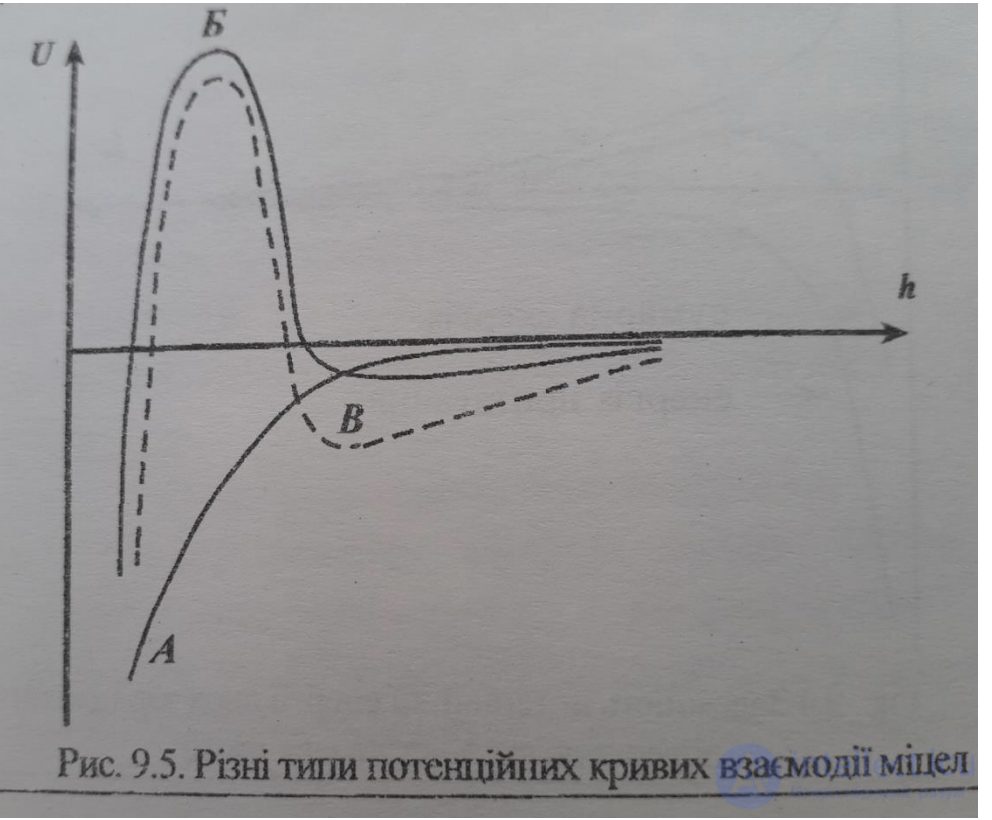
17. Форма залежності u - f(h) в конкретній КС визначається співвідношенням
параметрів в основному рівнянні. Є три варіанти характерних випадків.
А – бар’єра між міцелами або немає, або він малий, тому їх злипання неминуче.
В цій КС коагуляція необоротна.
Б – є високий бар’єр (umax>>kT), КС агрегативно стійка.
В – крім високого бар’єру є зона помітного притягнення, яка створює
«зворотний бар’єр», коли частинки, що попали в точку «Б», не можуть розійтись
під дією теплової енергії. Такі КС самоструктуруються.
18. Змінюючи концентрацію електроліту можна досягти стану, коли umax = 0 і
du/dh = 0. Це відповідає швидкій коагуляції, а Cmax = Υ. Тобто, згідно теорії
ДЛФО Υ=const/z
6
. Для йонів з Z=1,2,3 справедливим є співвідношення
1/Υ(Z=1):1/Υ(Z=2):1/Υ(Z=3) = 1:64:729.
На практиці в силу дії різних причин показник ступенів у Z змінюється від 2 до
6.
19. Особливості коагуляції під дією електролітів:
При дії суміші електролітів може бути або синергічний або антагоністичний
ефект.
Деякі багатозарядні йони за рахунок специфічної адсорбції можуть при
малих С визивати коагуляцію, а при високих – стабілізувати КС.
Свіжий осад можна пі дією пептизатора розчинити.
Коагулюючу силу електролітів можна зменшити дією ПАР. Захисна дія
найкраща у ВМС.
Исследование, описанное в статье про 6 : Устойчивость и коагуляция коллоидных систем, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое 6 : Устойчивость и коагуляция коллоидных систем и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Коллоидная химия и химия дисперсных систем
Комментарии