Лекция
Привет, Вы узнаете о том , что такое 2. Молекулярно – кинетические свойства коллоидных систем, Разберем основные их виды и особенности использования. Еще будет много подробных примеров и описаний. Для того чтобы лучше понимать что такое 2. Молекулярно – кинетические свойства коллоидных систем , настоятельно рекомендую прочитать все из категории Коллоидная химия и химия дисперсных систем.
1. Дифузія. Хаотичний тепловий рух молекул ДС обумовлює хаотичний
броунівський рух частинок ДФ. Для опису цього руху використовують
поняття сереньоквадратичного зсуву частинки ∆ за час τ.
Закон Ейнштейна – Смолуховського пов’язує ∆ з коефіцієнтом дифузії
(∆)2 = 2Dτ
Рух сферичних частинок описується рівнянням Стокса, тому
(∆)2 = (kБ
. Т
.
τ )/(3πηr), або D = kБ Т(6πηr)
Тут: η – в’язкість ДС, а r – радіус частинок ДФ.
2. Седиментація. Якщо густина ДФ і ДС різна, то в гравітаційному полі важкі
частинки ДФ будуть осідати.
Цей процес називається седиментацією.
У процесі руху частинок ДФ гравітаційна сила FГР. = mg урівноважується
силою тертя FТ = BU та архімедовою силою.
Для урівноваженого руху
(4/3)πr
3g∆ρ- 6πηrU = 0, тобто U =2g∆ρr2
/9η;
U/g = 2∆ρr2
/9η – константа седиментації
В центрифугах здійснюється примусова седиментація за рахунок того, що
a>>g. Об этом говорит сайт https://intellect.icu . Для розрахунку розподілу частинок ДФ користуються рівнянням:
ℓn Х/Х0 = 2 r
2∆ρω2
t/9η; Тут: ω- кутова швидкість; Х – відстань від центра
обертання.
3. За рахунок седиментації змінюється концентрація ДФ по висоті. Градієнт
концентрації, що виник, викликає дифузійний потік у протилежному
седиментації напрямі. При урівноваженні цих потоків встановлюється
дифузійно-седиментаційна рівновага, що характеризує кінетичну стійкість
КС. Розподіл частинок ДФ по висоті описується формулою Лапласа:
Ch = C0 exp( - Vg ∆ρh/ kБT)
В центрифузі:
ℓnС1 /С2 = V∆ρω2
(X1
2 – X2
2
)/ (2 kБT)
Кінетично седиментаційну стійкість оцінюють співвідношенням
КСС = 9η/2 r
2 ∆ρ
4. Седиментаційний аналіз КС Основою седиментаційного аналізу є залежність
швидкості осадження часток ДФ від їх розмірів. Використовують лише КС з
низькою концентрацією ДФ.
Для аналізу отримують седиментаційну криву – залежність маси осаду від τ .
Якщо КС монодисперсна залежність m від τ чітко лінійна
m = 2 r
2∆ρQτ/9ηH
Тут: m – маса осаду в момент часу τ; Q – загальна маса ДФ;
H- висота стовпа КС.
У випадку полідисперсних систем залежність m від τ нелінійна.
Тому використовують для аналізу метод дотичних
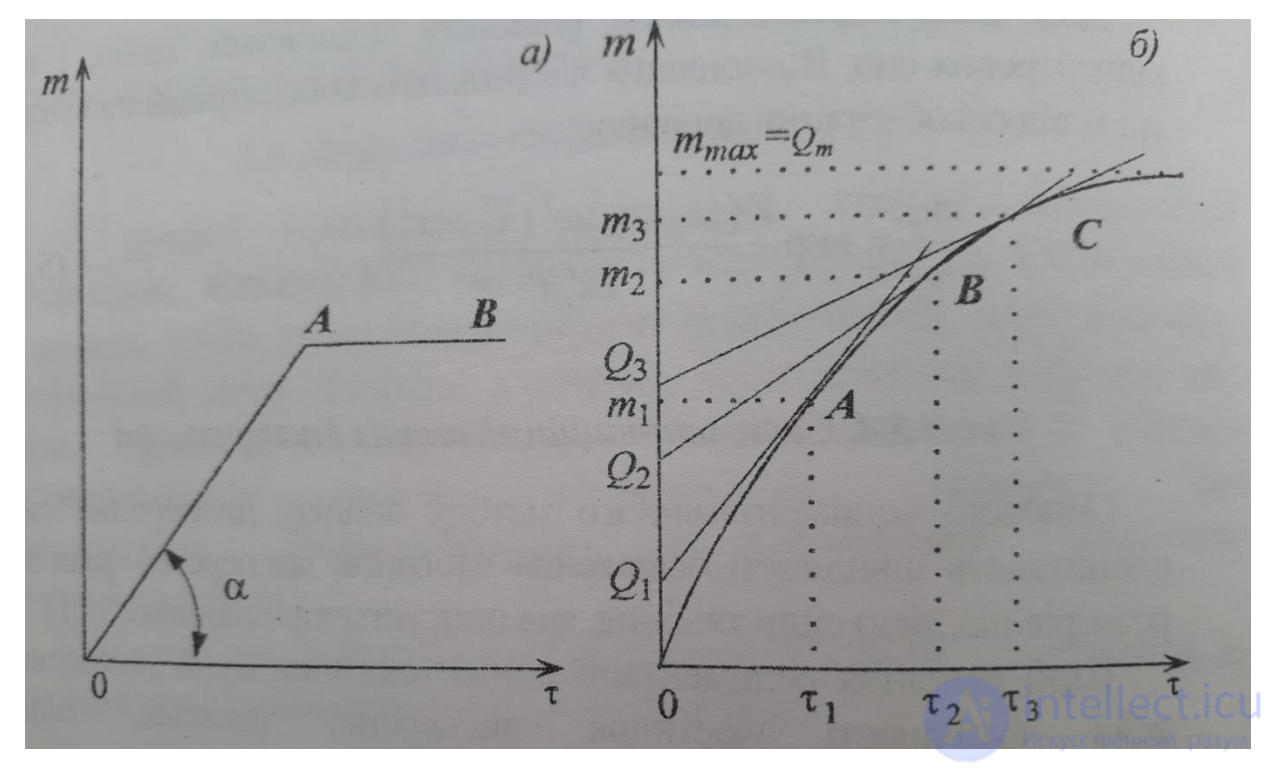
Розрахунки ведуться з використанням рівняння
ri = [(9ηHmi)/(2g∆ρQi τi)]1/2
На основі отриманих даних будують інтегральні та диференціальні криві
розподілу частинок за їх радіусами.
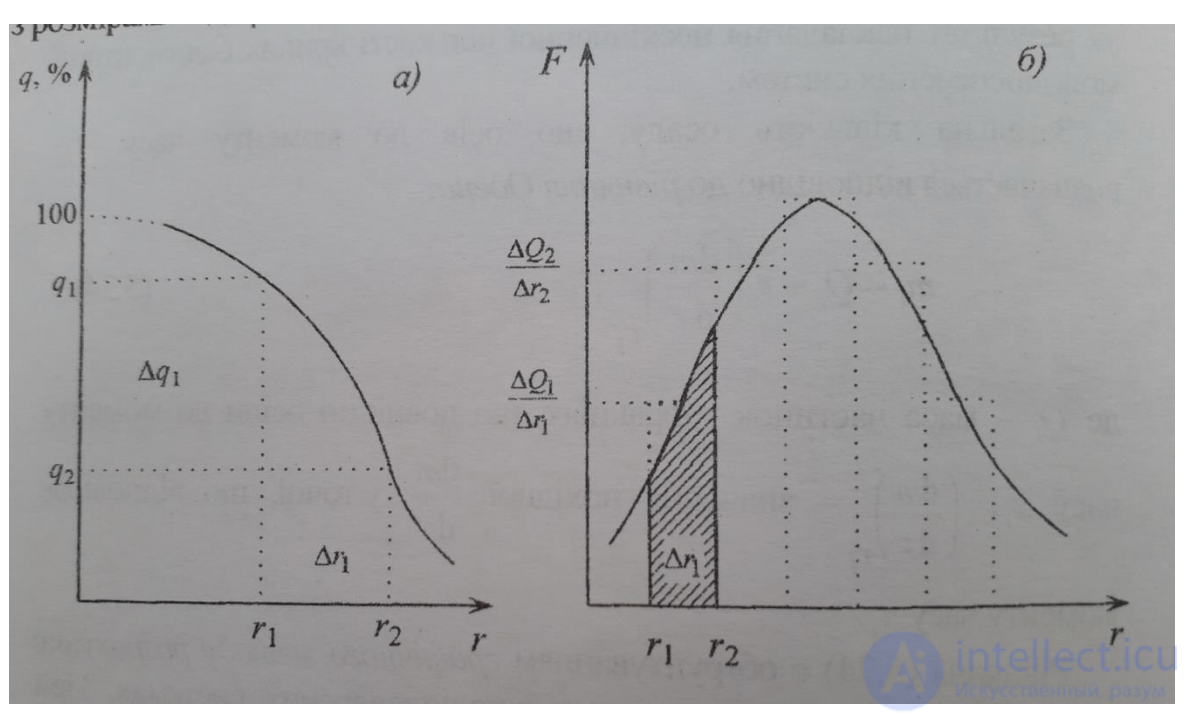
Для цього визначають qi = (Qi/Qmax)
. 100 і F = dq/qr ≈ ∆q/∆r
Исследование, описанное в статье про 2. Молекулярно – кинетические свойства коллоидных систем, подчеркивает ее значимость в современном мире. Надеюсь, что теперь ты понял что такое 2. Молекулярно – кинетические свойства коллоидных систем и для чего все это нужно, а если не понял, или есть замечания, то не стесняйся, пиши или спрашивай в комментариях, с удовольствием отвечу. Для того чтобы глубже понять настоятельно рекомендую изучить всю информацию из категории Коллоидная химия и химия дисперсных систем
Комментарии
Оставить комментарий
Коллоидная химия и химия дисперсных систем
Термины: Коллоидная химия и химия дисперсных систем